Применение диатомита
3. рабочий стандартный раствор железа с CFe3+ 0,005 мг/см3;
4. сульфосалициловая кислота, 10 %-ный раствор;
Ход определения
В колбу емкостью 50 мл наливают 20 мл анализируемого раствора, затем прибавляют пипеткой 2 мл раствора сульфосалициловой кислоты и, в зависимости от рН фильтрата, раствор соляной кислоты или аммиака; затем содержимое колбы тщательно перемешивают. Спустя 10 мин оптическую плотность окрашенного раствора измеряют с помощью КФК-2 на длине волны l=536—540 нм.
Приготовление и окрашивание, а затем и фотометрирование рабочей шкалы растворов сравнения производится по аналогичной схеме: 20см3 стандартного раствора + раствор сульфосалициловой кислоты и другие реактивы. Полученные значения D наносят на график против соответствующих концентраций железа в мг/л, и на основе этих данных строится калибровочная кривая, по которой определяют содержание трёхвалентного железа в фильтратах. Если значение оптической плотности исследуемого раствора выходит за пределы, обозначенные на графике, пробу следует разбавить и провести повторное фотометрирование.
Погрешность измерения оптической плотности на КФК-2 составляет 0,5% (±0,005).
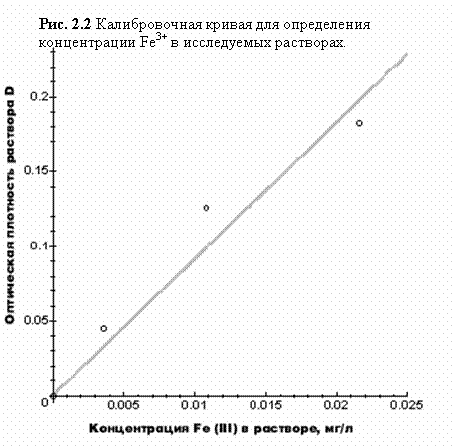 |
Таблица 2.4
Зависимость оптической плотности растворов сравнения от концентрации ионов Fe3+
| № раствора | 1 | 2 | 3 | 4 | 5 |
| С Fe3+, мг/л | 0 | 0,5 | 1,0 | 1,5 | 2,0 |
| D | 0 | 0,014 | 0,030 | 0,035 | 0,050 |
Определение значения рН исследуемых растворов
Во всех вышеперечисленных опытах вместе с определением концентраций ионов Al3+ и Fe3+ в исследуемых растворах изучалось влияние порошка диатомита на реакцию раствора. Проводилось измерение значений рН растворов извлечения и фильтратов потенциометрическим методом, и затем вычислялось ΔрН по формуле:
ΔрН=рНисх-рНф, где рНисх – значение рН раствора извлечения,
рНф – значение рН фильтрата.
Замеры рН проводились с использованием лабораторного рН-метра ЛПУ-01 с хлорсеребряным и стеклянным электродами соответственно в качестве электрода сравнения и измерительного электрода.
Нужное значение рН раствора извлечения в диапазоне от 1 до 13 устанавливалось путём прибавления к 1 М раствору хлористого калия разбавленных растворов соляной кислоты или аммиака.
Настройка рН-метра проводилась по буферным растворам с рН 1.68 (0,05 М раствор тетраоксалата калия), 6,86 (0,025 М раствор калия фосфорнокислого однозамещённого и 0,025 М раствор натрия фосфорнокислого двузамещённого) и 9,18 (0,01 М раствор натрия тетраборнокислого).
|
Погрешность измерения рН: |
в диапазоне рН 2-14 – ±0,04 в диапазоне рН -2-14 – ±0,40 |
2.4 Результаты исследований и обсуждение
Валовый химический состав исследуемого диатомита
По данным рентгеноспектрального анализа диатомит Инзенского месторождения, послуживший материалом для наших исследований, имеет химический состав, приведённый в таблице 2.5.
Таблица2.5
Химический состав диатомита Инзенского месторождения Ульяновской области
| Содержание, в % на сухую породу. | |||||||||
|
Na2O |
MgO |
Al2O3 |
SiO2 |
P2O5 |
SO2 |
K2O |
CaO |
TiO2 |
Fe2O3 |
|
0,01 |
0,07 |
5,35 |
90,20 |
0,09 |
0,03 |
0,12 |
0,70 |
0,12 |
3,22 |
По сравнению с цифрами, приведёнными в литературе, эта партия характеризуется повышенным содержанием кремнезёма (90,2% против 88,15% по данным У. Г. Дистанова; см. таблицу 1.1). Содержание полуторных окислов – в пределах среднего.
Опираясь на данные о содержании глинистого материала в породе, приводимые У. Г. Дистановым и другими авторами [25, 27], можно считать эти цифры косвенным подтверждением высокого содержания опалового кремнезёма в породе.
На основе полученных данных было рассчитано, что в 100 г диатомита в среднем содержится 2,83 г Al и 1,127 г Fe.
Выход алюминия из диатомита в зависимости от значения рН раствора извлечения
А) В ходе серии экспериментов было установлено, что нативный диатомит становится источником алюминия только при рН раствора извлечения менее 5,72 (±0,04) (интервал значений рНисх 1 – 10), а с уменьшением значения рН выход алюминия в раствор возрастает.
В) Для диатомита, прокалённого при 850°С, появление Al3+ в растворе отмечалось при рН<4,8.
Данные, отражающие зависимость CAl3+ в фильтрате от рН раствора извлечения, приведены в таблицах 2.6 и 2.7 и отражены на графиках, представленных на рисунках 2.1 и 2.2.
Таблица 2.6
Зависимость выхода алюминия от значения рН раствора извлечения для нативного диатомита
|
рН исх | 1,02 | 1,94 | 2,70 | 4,01 | 5,72 | 6,07 | 8,30 | 9,60 |
|
CAl3+, мг/см3 | 0,0175 | 0,0129 | 0,0033 | 0,0011 | 0,0000 | 0,0000 | 0,0000 | 0,0000 |
