Страница
2
Исследования, начатые Шейнбайном, продолжил А. Н. Бах, который в 1897 г. разработал перекисную теорию биологического окисления, приложив ее к процессам дыхания. Несколько позже, в том же 1897 г., аналогичные взгляды высказал немецкий исследователь К. Энглер.
Суть перекисной теории биологического окисления Баха заключается в следующем. Молекулярный кислород имеет двойную связь и для того чтобы его активировать, необходимо эту двойную связь расщепить. Легко окисляющееся соединение А взаимодействует с кислородом и, разрывая двойную связь, образует пероксид А02 Таким образом, по мысли Баха, активация кислорода есть образование пероксида. В свою очередь пероксидное соединение, взаимодействуя с соединением В, окисляет его; затем эта реакция повторяется со вторым атомом кислорода и второй молекулой соединения В. Получается полностью восстановленное исходное соединение — акцептор кислорода А и полностью окисленное вещество В.
Много позднее, в 1955 г., две группы исследователей — О. Хаяиши с сотр. в Японии и Г. С. Мэзон с сотр. в США, используя современные методы, проанализировали возможность включения кислорода в органические соединения.
В настоящее время известно, что путь включения кислорода в органические соединения в соответствии с перекисной теорией биологического окисления Баха и Энглера не имеет отношения к дыханию, однако работы этих исследователей сыграли большую роль в изучении химизма дыхания, заложив основы современного понимания механизмов активации кислорода.
История современного учения о дыхании растений неразрывно связана с именем академика В.И. Палладина.
В годы первого петербургского периода работы Палладин исследовал ферментативную природу дыхательного процесса. Палладин показал, что и анаэробная, и аэробная фазы дыхания обеспечиваются специфическими ферментами, последовательно перерабатывающими продукты дыхания. Итоги работ этого периода изложены в монографии В.И. Палладина «Дыхание как сумма ферментативных процессов» (1907).
Одновременно с Палладиным проблемой дыхания занимались в целом ряде крупнейших научно-исследовательских институтов и лабораторий Западной Европы. Наибольшую популярность приобрели две новые школы – Виланда и Варбурга.
Т. Виланд развивал взгляды на роль дегидраз и водородных акцепторов, вполне аналогичные взглядам Палладина. Расхождение их теорий заключалось в том, что Виланд категорически отрицал какую бы то ни было роль оксидаз как специфических активаторов кислорода, считая молекулярный кислород способным самостоятельно отнимать водород от водородного акцептора. По мнению же Палладина, водородные акцепторы не могут самопроизвольно освобождаться от водорода, но требуют для этого участия оксидаз, которые поэтому являются обязательным фактором в реакции, выраженной во втором уравнении Палладина.
Противник Виланда, Варбург, считал, что молекулярный кислород не может вступить в организме в какой бы то ни было окислительный процесс, если в организме отсутствует система железоорганических соединений, типичным представителем которых он считал геминфермент. Варбург утверждал, что геминфермент активирует молекулярный кислород, т.е. как бы дает первый толчок к началу окислительных процессов, и без него никакой дыхательный процесс не может совершаться. Далее, по мнению Варбурга, окислительный импульс через промежуточные звенья (геминовые соединения) доходит до дыхательного субстрата и окисляет его. Резюмируя свои взгляды, Варбург утверждал, что дыхание осуществляется путем активации кислорода, а отнюдь не водорода. Но ведь Палладин как раз и говорил о той же необходимости активации молекулярного кислорода, защищая перед Виландом роль оксидаз в процессе дыхания.
Все различие в основных посылках Варбурга и Палладина заключается в том, что первый, работая по преимуществу с объектами животного происхождения, называл свой активатор молекулярного кислорода геминферментом, а Палладин, работавший с объектами растительного происхождения, сохранил за этим активатором ранее установившееся в науке название оксидазы. Но по существу оба говорили об одном и том же, протестуя против непримиримой позиции Виланда, отрицавшего необходимость энзиматической активации молекулярного кислорода.
Английский биохимик Д. Кейлин в 1925 г. доказал присутствие в клетках цитохромоксидазы, ускоряющей поглощение ими кислорода, и открыл другие цитохромы. Затем цитохромы были обнаружены у всех аэробов и было показано, что у этих организмов на завершающем этапе процесса дыхания осуществляется перенос на кислород электронов и протонов, в результате чего образуется Н20 (или Н202).
3.Каталитические системы дыхания
Окисление дыхательных субстратов в ходе дыхания осуществляется с участием ферментов. Ферменты как белковые катализаторы, помимо свойств, присущих неорганическим катализаторам, обладают рядом особенностей: высокой активностью, высокой специфичностью по отношению к субстратам и высокой лабильностью. Их пространственная организации зависящая от нее активность изменяются под действием внешних и внутренних факторов. Эти свойства обеспечивают возможность тонкой регуляции обмена веществ на уровне ферментов.
Типы окислительно-восстановительных реакций. Существуют четыре способа окисления, и все они связаны с отнятием электронов:
1) непосредственная отдача электронов, например:
![]()
2) Отнятие водорода:
![]()
3) присоединение кислорода:
![]()
4) образование промежуточного гидратированного соединения с последующим отнятием двух электронов и протонов:
![]()
Оксидоредуктазы.
Поскольку окисление одного вещества (донора электронов и протонов) сопряжено с восстановлением другого соединения (их акцептора), ферменты, катализирующие эти реакции, называют оксидоредуктазами. Все они относятся к I классу ферментов:
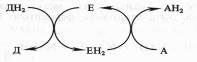
Донор (Д) отдает электроны и протоны, акцептор (А) принимает их, а энзим (Е) осуществляет реакцию переноса. Существуют три группы оксидоредуктаз:
а) анаэробные дегидрогеназы передают электроны различным промежуточным акцепторам, но не кислороду;
б) аэробные дегидрогеназы передают электроны различным акцепторам, в том числе кислороду;
в) оксидазы способны передавать электроны только кислороду.
Анаэробные дегидрогеназы. Это двухкомпонентные ферменты, коферментом которых может быть НАД+ (никотинамидадениндинуклеотид):
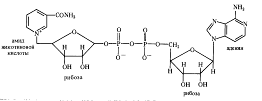
При окислении субстрата НАД+ превращается в восстановленную форму НАДH, а второй протон субстрата диссоциирует в среду (НАДH+ Н+). К анаэробным НАД-зависимым дегидрогеназам относятся такие ферменты, как алкогольдегидрогеназа, лактатдегидрогеназа, малатдегидрогеназа и др. Коферментом анаэробных дегидрогеназ может быть также НАДФ+ (никотинамидадениндинуклеотидфосфат), содержащий на одну фосфатную группировку больше, чем НАД + . НАДФ- зависимыми дегидрогеназами являются изоцитратдегидрогеназа, глюкозо-6-фосфатдегидрогеназа, 6-фосфоглюконатдегидрогеназа и др.
