Страница
2
В качестве примеров, иллюстрирующих использование протеоли-тических ферментов, можно привести белок полосы 3 эритроцитов, бактериородопсин, лактозопермеазу Е. coli и субъединицу IV цитохром с-оксидазы.
Иммунологические методы
Очень ценным инструментом для определения топографии мембранных белков являются специфичные антитела. В этом случае исследуют связывание антител с белками только в ориентированных мембранных препаратах типа мембранных везикул Е. coli. Анализ можно сделать количественным, если использовать соответствующие иммунологические методы. Места связывания можно локализовать с помощью электронной микроскопии, пометив антитела коллоидным золотом или используя золото, связанное со специфичным комплексом антиген—антитело на поверхности мембраны. Ясно, что в процессе приготовления мембранного препарата не должны разрушаться нативные топографические структуры. Чем точнее данные о местах связывания антител, тем информативнее будут эти эксперименты. Если исследовать ориентированные мембраны с нормальной или вывернутой ориентацией, то с помощью поли-клональных антител против определенного очищенного полипептидного фрагмента можно определить, имеет ли изучаемый белок участки, экспонированные на какой-либо одной стороне мембраны. Однако такие эксперименты не позволяют определить, какая часть белка экспонирована. Более детальную информацию можно получить с помощью двух подходов. Один состоит в использовании мо-ноклональных антител, а второй предусматривает применение поли-клональных антител против пептидов, соответствующих определенным областям белка.
Наиболее полезны те из них, которые связываются как с белком в мембране, так и с денатурированными фрагментами белка, что позволяет изучать белки после их разделения с помощью электрофореза в ПААГ в присутствии ДСН. Это особенно важно для локализации места связывания антител на полипептиде. В принципе эпитоп можно локализовать с точностью до нескольких аминокислотных остатков. В качестве примеров успешного использования моноклональных антител можно привести родопсин, бактериородопсин, ацетилхолиновый рецептор и белок LamB — рецептор фага X из наружной мембраны Е. coli.
Использование антител против синтетических пептидов, соответствующих отдельным белковым фрагментам, позволяет точно выяснить, доступна ли эта область белка для связывания антитела. Если антитела, специфичные к определенной аминокислотной последовательности, связываются с нативной формой белка в мембране, то исследователь получает мощный инструмент для определения топографии белка. Этим путем можно проверять отдельные топографические модели. Примерами успешного использования данного подхода являются работы по лактозопермеазе Е. coli, микросомному цитохрому Р450 и ацетилхолиновому рецептору. К сожалению, нет гарантий, что антипептндные антитела вообще будут связываться с белком. Потенциальный центр связывания в нативном белке может находиться в такой конформации или так быть упрятанным внутри белковой глобулы, что не будет узнан антителом или доступен для него. Действительно, в некоторых случаях антипептидные антитела не связываются с белком даже после его денатурации в ДСН.
Весьма остроумным является подход к определению топографии полипептида, основанный на методах молекулярной генетики. Он состоит во введении чужеродного эпитопа в аминокислотную последовательность мембранного белка с последующим использованием антител, специфичных к этому эпитопу.
Химическая модификация
Этот подход широко использовался для локализации белков или их отдельных участков на поверхности мембраны или в ее гидрофобной области. Белок вступает в реакцию с реагентом, который может действовать лишь на одной стороне ориентированной мембраны или в ее гидрофобной сердцевине. Реагент, предназначенный для идентификации белка на поверхности мембраны, должен быть сильно полярным; он не должен адсорбироваться на мембране или накапливаться внутри ее. Для локализации же той части белка, которая находится в контакте с углеводородными хвостами липидных молекул, следует использовать очень неполярные реагенты, которые концентрируются в гидрофобной области мембраны. Артефакты, возникающие при этом подходе, чаще всего бывают связаны с тем, что реагент модифицирует белок не только в том реакционном пространстве, для которого он был предназначен. Например, реагент, направленный на модификацию поверхности мембраны, может иметь достаточно неполярный характер, чтобы проникать через мембрану и получать доступ к белкам внутреннего компартмента. Химическая модификация может также привести к повреждению мембраны и сделать ее проницаемой для того реагента, который, как ожидается, должен быть непроникающим. В табл. 1 перечислены некоторые из химических реагентов, используемые для изучения топографии мембранных белков.
Модификацию белков на поверхности мембраны часто проводят с помощью фермента лактопероксидазы, которая катализирует иодирование доступных остатков тирозина или гистидина. Поскольку реакция между I" и Н2О2 происходит в активном центре лактопероксидазы, последняя должна быть в высшей степени «векторной», т.е. локализованной только на одной стороне мембраны. Однако при определенных условиях в ходе реакции может образовываться Ь, который, проникая через мембрану, способен иодировать аминокислотные остатки на внутренней стороне мембраны. Это показывает, насколько важен строгий контроль условий протекания реакций для исключения артефактов.
Для поверхностной модификации часто используются и другие реагенты — соли диазония, которые реагируют с боковыми цепями остатков лизина, цистеина, тироксина и гистидина, а также фотоак-тивируемые реагенты, например NAP-таурин.
В табл. 1 перечислен также ряд неполярных фотоактивируемых реагентов, которые используются для избирательной модификации аминокислотных остатков белка, контактирующих с гидрофобной областью бислоя. Эти реагенты обычно добавляют к мембранному препарату, дают им возможность накопиться в бислое и затем подвергают их фотоактивации. Преимущество образующихся при этом нитренов и карбенов состоит в том, что их реакции намного менее специфичны по сравнению с реакциями других активных частиц, так что ковалентная модификация не ограничивается боковыми цепями каких-либо определенных аминокислот. Правда, нитрены проявляют избирательность по отношению к нуклеофилам. Использование карбенов предпочтительнее, поскольку они вступают в реакцию с более высоким выходом. Для получения информации о вторичной структуре трансмембранных участков полипептидной цепи путем определения тех остатков, которые контактируют с липидами, использовали реагент ТИД. Например, спираль С бак-
Таблица 1. Некоторые реагенты, применяемые для изучения топографии мембранных белков
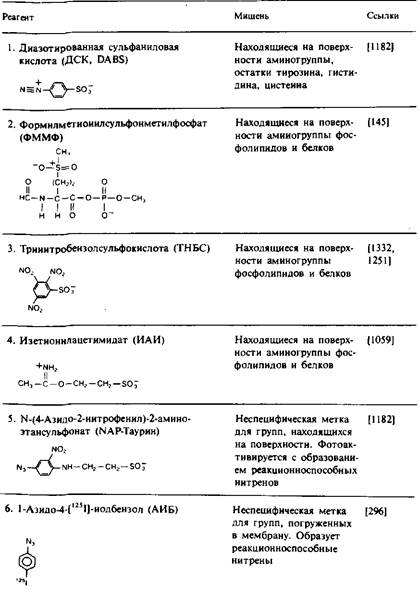

териородопсина включает метку лишь с одной стороны; это согласуется с представлением о том, что данная спираль является трансмембранной, причем ее неполярная область обращена в липидную фазу.
