Страница
4
Вторую подгруппу составляют в большинстве аэробные ацидофильные формы. Оптимальный pH их роста лежит ниже 4,5 (2 – 3). В этих условиях Fe2+ в присутствии O2 устойчиво к химическому окислению. Для ацидофильных железобактерий установлена способность получать энергию в результате окисления двухвалентного железа.
Основным представителем бактерий с энергетическим метаболизмом хемолитотрофного типа является Thiobacillusferrooxidans, относящийся к группе тионовых бактерий и обладающий способностью получать энергию также в результате окисления различных восстановленных соединений серы. Окислять закисное железо с получением клеткой энергии способна и облигатно ацидофильная бактерия Leptospirillumferooxidans, близкая по ряду свойств к T. ferooxidans, но в отличии от последнего не окисляющая соединения серы.
Leptospirillumferooxidans и большинство изученных штаммов T. ferooxidans принадлежат к облигатным хемолитоавтотрофам, использующим энергию окисления железа для ассимиляции CO2, служащей основным или единственным источником углерода. Некоторые штаммы T. ferooxidans оказались способными расти на средах с органическими соединениями, являясь, таким образом, факультативными хемолитотрофами. Наконец, описаны термофильные бактерии, получающие энергию в результате окисления Fe2+ и нуждающиеся для роста в органических соединениях, т. е. осуществляющие метаболизм хемолитотрофного типа.
Окисление железа, приводящее к получению энергии, происходит в соответствии с уравнением
2Fe2+ + 1/2O2 + 2H+ ® 2Fe3+ + H2O,
что сопровождается незначительным изменением уровня свободной энергии (DG¢o при pH=2 равно – 33 кДж/моль). Поэтому для обеспечения энергией клетке необходимо «переработать» большие количества железа.
Механизм окисления Fe2+ в дыхательной цепи изучен у T. ferooxidans. Дыхательная цепь этой бактерии содержит все типы переносчиков, характерные для дыхательной системы аэробных хемоорганотрофных эубактерий, но участок цепи, связанный с получением энергии, очень короток.
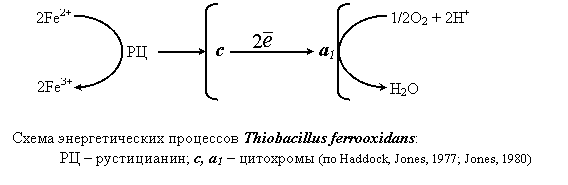 |
Окисление Fe2+ происходит на внешней стороне цитоплазматической мембраны; в цитозоль через мембрану железо не проникает. Электроны с Fe2+ акцептируются особым медьсодержащим белком – рустицианином, находящимся в периплазматическом пространстве.
Затем с рустицианина они передаются на цитохром c, локализованный на внешней стороне цитоплазматической мембраны, а с него на цитохром a1, расположенный на внутренней стороне мембраны. Перенос электронов с цитохрома a1 на 1/2O2, сопровождающийся поглощением из цитоплазмы 2H+, приводит к восстановлению молекулярного кислорода до H2O. Особенность дыхательной цепи T. ferrooxidans – отсутствие переноса через мембрану протонов, а перенос только электронов. Градиент H+ по обе стороны цитоплазматической мембраны поддерживается как за счет поглощения протонов из цитоплазмы, так и в результате низкого pH внешней среды, в которой обитают эти бактерии. Синтез АТФ происходит за счет движения H+ из внешней среды в цитоплазму через АТФ-синтазный комплекс. Движущей силой служит в основном DpH. Для синтеза 1 молекулы АТФ необходимо окислить как минимум 2 молекулы Fe2+.
Образование восстановителя происходит в результате энергозависимого обратного переноса электронов. Активность участка дыхательной цепи, обеспечивающей обратный электронный транспорт, на порядок ниже активности короткого участка, функционирование которого приводит к получению энергии. В целом для фиксации 1 молекулы CO2 в восстановительном пентозофосфатном цикле необходимо окислить больше 22 молекул Fe2+. Таким образом, из всех представителей эубактерий, у которых обнаружена способность к окислению железа, только облигатно ацидофильные формы могут использовать энергию окисления Fe2+ для ассимиляции CO2, т. е. существовать хемолитоавтотрофно. Именно они являются истинными железобактериями, соответствуя тому названию, которое было введено С.Н. Виноградским.
Для остальных организмов образование окислов железа не связано с получением энергии и происходит в результате неспецифических реакций ионов металлов с продуктами метаболизма, прежде всего продуктами неполного восстановления O2.
Эубактерии, описанные здесь, широко распространены в природе и могут существовать в большом диапазоне условий. Облигатные ацидофилы обнаружены в подземных водах сульфидных месторождений, кислых водах железистых источников и кислых озерах с высоким содержанием закисного железа. Нитчатые формы также занимают вполне определенные экологические ниши. Представители рода Leptothrix – обитатели олиготрофных железистых поверхностных вод, Sphaerotilus предпочитают среды с высоким содержанием органических веществ. Скопления отмерших железобактерий (гидрат окиси железа) образуют на дне стоящих водоемов залежи болотных руд, количество которой может достигать огромных размеров.
Заключение.
Рассмотренные в этом реферате микроорганизмы широко распространены в природе, некоторые из них применяются в сельском хозяйстве и в промышленности. Однако большинство из этих организмов пока имеют лишь научный интерес. Это связано с тем, что бактерии обитают в очень специфических условиях, многие из них только недавно получены в чистом виде.
Микромир океанских глубин еще малоизучен, постоянно открываются новые виды микроорганизмов. На современном этапе развития научно-технического прогресса становится возможным изучение бактерий в их естественной среде обитания (в частности серобактерий геотермальных вод на глубинных океанических разломах).
В будущем, с истощением ископаемого органического топлива, возможно, будут открыты (или получены) бактерии способные в промышленных масштабах получать энергию путем метаболизма неорганических веществ.
Список литературы:
1. Асонов Н.Р. Микробиология. М.: Колос. 1989.
2. Бейли, Дж. Э, Оллис, Дэвид Ф Основы биохимической инженерии. М.1989.
3. Гусев М.В., Минеева Л.А. Микробиология: Учебник. М.: Изд-во МГУ,1992.
4. Мишустин Е.Н., Емцев В.Т. Микробиология. М.:Колос.1978.
5. Шлегель Г. Общая микробиология. М.: Мир.1987.
