Страница
10
В 1939—1940 гг. Ф. Липман установил, что АТФ служит главным нереносчиком энергии в клетке. Особые свойства этого вещества определяются тем, что конечная фосфатная группа легко переноситься с АТФ на другие соединения или отщепляется с выделением энергии, которая может быть использована на физиологические функции. Эта энергия представляет собой разность между свободной энергией АТФ и свободной энергией образующихся продуктов (AG). AG — это изменение свободной энергии системы или количество избыточной энергии, которая освобождается при реорганизации химических связей. Распад АТФ происходит по уравнению AТФ + Н20 = АДФ + ФН, при этом происходит как бы разрядка аккумулятора, при рН 7 выделяется AG = —30,6 кДж. Этот процес катализируется ферментом аденозинтрифосфатазой - (АТФ-аза) Равновесие гидролиза АТФ смещено в сторону завершения peaкции, что и обусловливает большую отрицательную величину свободной энергии гидролиза. Это связано с тем, что при диссоциации. Четырех гидроксильных группировок при рН 7 АТФ имеет четыре отрицательных заряда. Близкое расположение зарядов друг к другу способствует их отталкиванию и, следовательно, отщеплению фосфатных группировок. В результате гидролиза образуются соединения с одноименным зарядом (АДФ3~ и НР04~), которые отживаются друг от друга, что препятствует их соединению. Уникальные свойства АТФ объясняются не только тем, что при ее гидролизе выделяется большое количество энергии, но и тем, что она обладает способностью отдавать концевую фосфатную группу вместе с запасом энергии на другие органические соединения. Энергия, заключенная в макроэргической фосфорной связи, используется на физиологическую деятельность клетки. Вместе с тем по величине свободной энергии гидролиза — 30,6 кДж/моль АТФ занимает промежуточное положение. Благодаря этому система АТФ — АДФ может служить носчиком фосфатных групп от фосфорных соединений с более высокой энергией гидролиза, например фосфоенолпируват (53,6 К/моль), к соединениям с более низкой энергией гидролиза, пример сахарофосфатам (13,8 кДж/моль). Таким образом, система АДФ является как бы промежуточной или сопрягающей.
Механизм синтеза АТР. Сопряжение диффузии протонов назад через внутреннюю мембрану митохондрии с синтезом АТР осуществляется с помощью АТРазного комплекса, получившего название фактора сопряжения F,. На электронно- микроскопических снимках эти факторы выглядят глобулярными образованиями грибовидной формы на внутренней мембране митохондрий, причем их «головки» выступают в матрикс. F1 — водорастворимый белок, состоящий из 9 субъединиц пяти различных типов. Белок представляет собой АТРазу и связан с мембраной через другой белковый комплекс F0, который перешнуровывает мембрану. F0 не проявляет каталитической активности, а служит каналом для транспорта ионов Н+ через мембрану к Fx.
Механизм синтеза АТР в комплексе Fi~ F0 до конца не выяснен. На этот счет имеется ряд гипотез.
Одна из гипотез, объясняющих образование АTP посредством так называемого прямого механизма, была предложена Митчеллом.
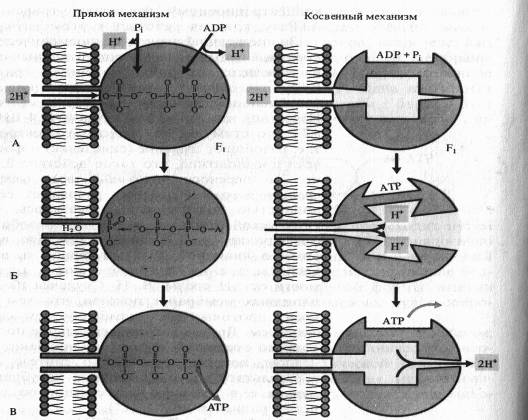
По этой схеме на первом этапе фосфорилирования фосфатный ион и ADP связываются с г компонентом ферментного комплекса (А). Протоны перемещаются через канал в F0-компоненте и соединяются в фосфате с одним из атомов кислорода, который удаляется в виде молекулы воды (Б). Атом кислорода ADP соединяется с атомом фосфора, образуя АТР, после чего молекула АТР отделяется от фермента (В).
Для косвейного механизма возможны различные варианты. ADP и неорганический фосфат присоединяются к активному центру фермента без притока, свободной энергии. Ионы Н + , перемещаясь по протонному каналу по градиенту своего электрохимического потенциала, связываются в определенных участках Fb вызывая конформационныё. изменения фермента (П. Бойер), в результате чего из ADP, и Р( синтезируется АТР. Выход протонов в матрикс сопровождается возвратом АТР-синтетазного комплекса в исходное конформационное состояние и освобождением АТР.
В энергизованном виде F1 функционирует как АТР-синтетаза. При отсутствии сопряжения между электрохимическим потенциалом ионов Н+ и синтезом АТР энергия, освобождающаяся в результате обратного транспорта ионов Н+ в матрикс, может превращаться в теплоту. Иногда это приносит пользу, так как повышение температуры в клетках активирует работу ферментов.
7.Митохондрии как органоиды дыхания. Их структура и функции
Митохондрии — «силовые» станции клетки, в них локализована большая часть реакций дыхания (аэробная фаза). В митохондриях происходит аккумуляция энергии дыхания в аденозинтрифосфате (АТФ). Энергия, запасаемая в АТФ, служит основным источником для физиологической деятельности клетки. Митохондрии обычно имеют удлиненную палочковидную форму длиной 4—7 мкм и диаметром 0,5-2 мкм.Число митохондрий в клетке может быть различным, от 500 до 1000. Однако в некоторых организмах (дрожжах) имеется лишь одна гигантская митохондрия. Химический состав митохондрий несколько колеблется. В основном это белковолипоидные органеллы. Содержание белка в них составляет 60—65%. В состав мембран митохондрий входят 50% структурных белков и 50% ферментативных, около 30% липидов. Очень важно, что митохондрии содержат нуклеиновые кислоты: РНК—1% и ДНК—0,5%. В митохондриях имеется^ не только ДНК, но и вся система синтеза белка, втом числе и рибосомы. Митохондрии окружены двойной мембраной? Толщина мембран составляет 6—10 нм. Между мембранами — перимитохондрлальное пространство, равное 10 нм; оно заполнено жидкостью типа сыворотки. Внутреннее пространство митохондрий заполняет матрикс в виде студнеобразной полужидкой массы. В матриксе сосредоточены ферменты цикла Кребса.
Внутренняя мембрана дает выросты — кристы, расположенные перпендикулярно продольной оси органеллы и перегораживающие все внутреннее пространство митохондрий на отдельные отсеки. Однако, поскольку выросты-перегородки неполные, между этими отсеками сохраняется связь. Мембраны митохондрий обладают большой прочностью и гибкостью. Во внутренней мембране локализована дыхательная цепь (цепь переноса электронов). На внутренней мембране митохондрий расположены грибовидные частицы. Они расположены через правильные промежутки. Каждая митохондрия содержит 104—105 таких грибовидных частиц. Установлено, что в головке грибовидных частиц содержится фермент АТФ-синтетаза, катализирующий образование АТФ аа_счет Энергий, выделяющейся в аэробной фазе дыхания.
Митохондрии способны к движению. Это имеет большое значение в жизни клетки, так как митохондрии передвигаются к тем местам, где идет усиленное потребление энергии. Они могут ассоциировать друг с другом как путем тесного сближения, так и при помощи связующих тяжей. Наблюдаются также контакты митохондрий с эндоплазматической сетью, ядром, хлоропластами. Известно, что митохондрии способны к набуханию, я при потере воды — к сокращению.
В растущих клетках митохондриальный матрикс становится менее плотным, количество крист растет — это коррелирует с увеличением интенсивности дыхания. В процессе дыхания ультраструктура митохондрий меняется. В том случае, если в митохондриях протекает активный процесс преобразования энергии окисления в энергию АТФ, внутренняя часть митохондрий становится более компактной.
