Модели системы кровообращения
Еще более интересной представляется возможность количественного прогнозирования функциональной прочности организма в условиях повышенной весомости, в частности при использовании различных средств компенсации. Для решения этой задачи рассмотренная модель кровообращения нуждается в двух модификациях. Первая, более простая, состоит в уточнении некоторых аналитических соотношений (прежде всего регуляторных) и числовых параметров модели, вторая - в выборе критерия функциональной прочности, учитывающего состояние сознания и уровень работоспособности. Критичным в этом плане является кровоснабжение головного мозга, так что искомый критерий К будет функцией одного или нескольких показателей мозгового кровотока (например, давления крови в тканях мозга, кровенаполнения и/или объемного кровотока).
Пусть в i-ом модельном эксперименте значение величины К (t) упало до уровня Ki* к моменту времени, когда в реальных условиях возникли нарушения сознания и недопустимое снижение работоспособности оператора. Среднее значение K*, полученное при моделировании ряда экспериментальных режимов, даст искомый критерий. Если теперь при модельном анализе нового режима воздействия окажется, что расчетное значение К (t) во всех случаях превышает критическое K*, то можно с некоторой вероятностью считать рассматриваемое воздействие переносимым, а используемые средства компенсации - эффективными.
Использование такого качественного критерия типа "допустимого-недопустимого" представляет определенный практический интерес, но более перспективным было бы использование вероятностного прогнозирования функциональной прочности в условиях повышенной весомости с учетом результатов статического моделирования переносимости, описанного выше.
Следует помнить, что описанная модель может оказаться слишком грубым инструментом для столь подробного количественного исследования. Выявление вероятностных зависимостей между параметрами мозгового кровообращения и состоянием сознания целесообразно проводить, используя более подробное описание особенностей сосудистого русла и механизмов регуляции, прежде всего мозгового кровообращения. [1]
Упрощенная модель системы кровообращения
В упрощенной модели системы кровообращения каждая цепь (как малого, так и большого круга кровообращения) имеет одинаковую структуру и состоит из линейных объемных податливостей (СА для артерии и Сv для вены), связанных на периферии через линейное сопротивление, описываемое уравнением Пуазейля.
Для людей молодого возраста (16-39 лет) объемная податливость CAS=1 мл/ (мм рт. ст). Объемную податливость вен большого круга можно оценить, если принять, что при кратковременной остановке сердца среднее системное давление равно примерно 10 мм рт. ст., а весь объем циркулирующей крови (5 литров) сосредоточен в венах большого круга. Отсюда CAS≈500 мл/ (мм рт. ст).
Оценить величину периферического сопротивления (RS) большого круга можно, предположив, что средние значения давлений в артериальном и венозном резервуарах равны соответственно 100 и 20 мм рт. ст.; средняя величина минутного кровообращения 5 л/мин.
Отсюда RS = 20 (мм рт. ст) / (л/мин).
В упрощенной гидравлической модели системы кровообращения (рис.3) один механический насос (левый) перекачивает кровь из легочной вены в артерию большого круга со скоростью QL, а второй (правый) перекачивает кровь из вены большого круга в легочную артерию со скоростью QR. Индексы A и V относятся, соответственно, к артерии и вене, а P и S - к цепям малого и большого кругов. Система содержит фиксированный объем крови B, распределенный между четырьмя резервуарами, причем предполагается, что объем насосов и связывающих их трубок пренебрежительно мал.
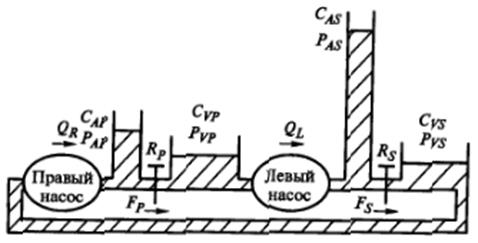
Рис.3. Гидравлический аналог системы кровообращения.
Весьма просто записать систему уравнений, описывающих работу этого аналога. Сначала сформулируем уравнение неразрывности для каждого из четырех резервуаров. Так скорость изменения объема крови в артерии большого круга BAS равна разности между скоростью притока QL и скоростью оттока FS. Но поскольку податливость артерии CAS равна, по определению, отношению объема к давлению (т.е. CAS =BAS/PAS), то очевидно, что BAS = CAS PAS.
Следовательно, имеем CAS PAS = QL - FS.
Для каждого из оставшихся трех резервуаров могут быть записаны аналогичные уравнения:
CVSBVS=-QR+FS; (1)
CAPPAP=QR-FP; (2)
CVPPVP=-QL+FP. (3)
Далее запишем уравнения Пуазейля:
FS = (PAS - PVS) / RS; (4)
FP = (PAP - PVP) / RP; (5)
Подставляя уравнения (4) - (5) в уравнения (1) - (3) и приводя их к общему знаменателю, получим:
RSCASPAS + (PAS - PVS) = RSQL; (6)
RSCVSPVS - (PAS - PVS) = - RSQR; (7)
RPCVSPVP + (PAP - PVP) = RPQR; (8)
RPCVPPVP - (PAP - PVP) = - RPQL. (9)
Описанная упрощенная структурная схема системы кровообращения является основой многих математических и физических моделей, используемых для исследования регуляции кровообращения, в клинической практике для идентификации индивидуальных (для конкретного пациента) параметров насосной функции сердца, центрального и периферического кровообращения, в лабораторных исследованиях конструкций протезов сосудов, искусственных клапанов и желудочков сердца.
Количественной характеристикой течения крови является линейная скорость кровотока, т.е. скорость перемещения малого объема крови, размер которого намного меньше сосуда. [8]
Заключение
Исследование структуры системы кровообращения и механических процессов, происходящих в отдельных ее элементах, дает возможность строить различные математические модели функционирования системы в целом, подобные приведенным ранее, и решать с помощью этих моделей некоторые теоретические и практические задачи. Например, предсказывать реакцию системы на перегрузки или падение внешнего давления, анализировать гипотезы о механизмах регуляции, изучать распространение метаболитов, кислорода, лекарственных веществ и индикаторов в организме и т.д.
Термин "моделирование" означает здесь в сущности решение достаточно сложной системы уравнений ЭВМ. Для проведения такого исследования необходимо знать эти уравнения, граничные и начальные условия и числовые значения определяющих параметров.
Физическое моделирование системы кровообращения, к которому, кроме экспериментов на гидравлических устройствах, нужно отнести еще и опыты, поставленные на животных одного вида с целью применить результаты к животным других видов, выдвигает ряд совершенно иных проблем, главная из которых - установление взаимосвязи между параметрами модели и реального объекта.
Поскольку деятельность сердечно-сосудистой сиcтемы и деятельность других физиологических систем тесно связаны друг с другом, то может быть поставлен вопрос об основных универсальных принципах этой связи. Ряд исследователей склоняется к мысли, что эволюция развития животных могла привести к некоторой оптимальной (в термодинамическом смысле) организации физиологических систем, такой, что, например, связь между процессами кроветворения и, дыхания и кровообращения определяется условием оптимального снабжения тканей кислородом. Постулируя оптимальность такого рода, можно провести расчеты некоторых заранее неочевидных соотношений между параметрами системы и сопоставить затем результаты с опытными данными для проверки исходной гипотезы. [5,6]
