Страница
4
3.4.3 ЯМР-спектроскопия
Этот метод также может использоваться для изучения мембранных белков. Однако возможности метода в этом случае ограничены, что связано главным образом с относительно медленными движениями интегральных мембранных белков in situ и в комплексах с детергентом.
3.5 Определение ферментативной активности
Одним из наиболее важных методов характеристики очищенных мембранных белков несомненно является определение биохимической активности. При этом используются в основном такие же критерии, как и для растворимых белков, но могут возникать и свои трудности. Первая из них связана с тем, что биохимическая активность мембранных белков часто очень сильно зависит от связывания с белком липидов и детергентов. Потеря активности может быть как обратимой, так и необратимой. Целесообразно иметь какую-то оценку удельной активности исследуемого белка in vivo или в составе мембран до солюбилизации. Избыток детергента может оказывать ингибирующий эффект, например за счет разбавления неполярных субстратов в популяции мицелл и уменьшения ферментативной активности. Измеряя активность любого мембранного белка, необходимо иметь в виду, что in situ он находится в окружении липидов, обеспечивающих оптимальную активность. Вторая проблема связана с белками, обладающими "трансбислойной" активностью; примерами могут служить белки, образующие каналы, и транспортные белки. В этих случаях необходимо учитывать перемещение растворенных веществ из одного компартмента в другой (например, внутрь липосом и наружу).
3.6 Изучение стехиометрии субъединиц
Многие мембранные ферменты представляют собой комплексы, состоящие из нескольких субъединиц. В качестве примера можно привести Н + - АТРазу, Na +/ К + - АТРазу, митохондриальные комплексы электронного транспорта и фотосинтетические реакционные центры. Некоторые интегральные мембранные белки прочно связаны с растворимыми белками с помощью нековалентных взаимодействий (примерами могут служить Fo - и F1-компоненты митохондриальной Н + - АТРазы). В Е. сoli Fo-компонент, содержащий по данным электрофореза в ПААГ-ДСН три типа субъединиц (а, b, с), образует протонный канал, a F1, состоящий из пяти типов субъединиц, содержит активный центр, участвующий в гидролизе АТР. Для таких белков очень важно определить характер субъединиц, стехиометрию комплекса и ближайшие взаимодействия его компонентов. Это весьма непростая задача даже тогда, когда белковый комплекс уже изолирован. Возникающие здесь проблемы по существу не отличаются от таковых для растворимых белковых комплексов, но имеются и свои дополнительные сложности.
Прежде всего следует иметь в виду, что взаимодействие между субъединицами очень сильно зависит от типа липидов и детергентов, с которыми связаны белки.
Еще одна проблема связана с тем, что в бислое мембранные белки могут образовывать комплексы из-за высокой их локальной концентрации. При солюбилизации же независимо от используемого детергента может произойти разбавление мембранных белков и их разъединение. По закону действующих масс это приведет к диссоциации комплексов, в которых взаимодействие между компонентами не очень сильное.
Для изучения стехиометрии субъединиц и их ассоциации в очищенном комплексе используется всего несколько методов:
1) химическое сшивание;
2) количественный анализ N-концевых аминокислот;
3) определение отношения массы субъединиц в ДСН-полиакриламидных гелях путем определения интенсивности окрашивания, с помощью радиоавтографии или иммуноблоттинга.
Каждый метод имеет свои ограничения, но все они использовались на практике.
3.7 Изучение трехмерной структуры с помощью рентгеновской дифракции и реконструкции изображения
3.7.1 Кристаллизация мембранных белков
Наиболее детальную структурную информацию об очищенных мембранных белках можно получить, исследуя методом рентгеновской дифракции трехмерные белковые кристаллы. К сожалению, оказалось, что интегральные мембранные белки очень трудно кристаллизовать. Будучи удалены из своего естественного липидного окружения, неполярные участки липидных молекул склонны агрегировать с образованием неупорядоченных форм, непригодных для кристаллографического анализа. Ясно, что необходимы специальные методы, позволяющие обойти эти трудности, и в этом был достигнут определенный прогресс. Михель обратил внимание, что мембранные белки образуют кристаллы двух типов (рис.2).
Кристаллы типа I напоминают стопки мембран. В них осуществляется латеральное взаимодействие между неполярными участками, а мембраноподобные слои связывают полярные участки белков. Подобные кристаллы были получены для нескольких белков, но ни в одном случае их нельзя было исследовать с помощью дифракции с высоким разрешением. Кристаллы типа II стабилизируются за счет контактирования полярных участков белковых молекул, а небольшие амфифильные соединения или детергенты в основном заполняют промежутки между ними. Заметим, что очень важными являются размер, заряд и другие свойства детергентов; если эти параметры неблагоприятны, то детергент может дестабилизировать кристаллическую структуру. Кристаллы типа II образуют белки фотосинтетического реакционного центра Rhodopseudomonas viridis
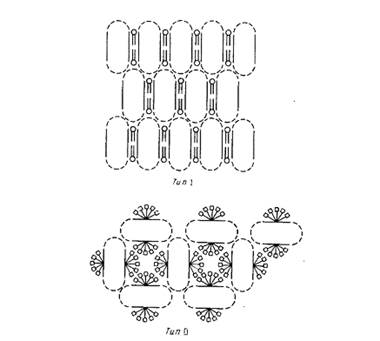
Рис.2. Два основных типа кристаллов мембранных белков.
Кристаллы типа I представляют собой двумерные стопки, упорядоченно расположенные в третьем измерении. В кристаллах типа II с гидрофобными поверхностями белков связаны молекулы детергента. Пунктиром отмечены гидрофильные домены белков.
Итак, мембранные белки можно кристаллизовать, и хотя число успешных попыток пока невелико, можно сделать несколько выводов, касающихся методологии кристаллизации.
1. Белки кристаллизуются вместе с детергентом.
2. Очень важен выбор детергента. По-видимому, наиболее пригодны цвиттерионные или неионные детергенты с высокой ККМ и малым размером мицелл
3. Кристаллизация облегчается в присутствии малых амфифильных органических молекул, по-видимому, влияющих на полярные концевые группы детергента.
4. Полиэтиленгликоль и сульфат аммония, обычно использующиеся при кристаллизации растворимых белков, применяются и для индукции кристаллизации мембранных белков.
3.7.2 Реконструкция изображения и двумерные кристаллы
Трехмерные кристаллы мембранных белков получить очень трудно, но многие из них образуют двумерные упорядоченные структуры. В некоторых случаях белки формируют такие структуры in vivo, (например, бактериородопсин в пурпурной мембране). При подходящих условиях такие белки, как и многие другие, образуют "двумерные кристаллы" при их очистке и реконструкции в присутствии фосфолипидов. Подобные двумерные упорядоченные структуры можно, использовать для получения трехмерной структурной информации с помощью электронной микроскопии и методов реконструкции изображения.
4. Пример структурных исследований мембранных белков.
4.1 Структура поринов
