Водные растворы электролитов
Если a мала, то 1- a ≈ 1 и тогда
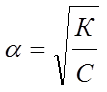 .
.
Видно, что с уменьшением концентрации электролита в растворе степень электролитической диссоциации возрастает.
Диссоциация слабого электролита, молекула которого может диссоциировать не на два, а на большее количество ионов (электролиты с разновалентными ионами), протекает по стадиям (ступенчатая диссоциация). Например, при диссоциации слабой угольной кислоты Н2СО3 в водном растворе имеют место следующие равновесия:
I стадия: Н2СО3 <=> Н+ + НСО3-
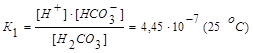 .
.
II стадия: НСО3- <=> Н+ + СО32-
 .
.
Как видно из этих данных, процесс диссоциации слабого электролита с разновалентными ионами определяется главным образом первой ступенью.
Для примера приведем константы электролитической диссоциации некоторых слабых кислот и оснований (25 °С):
|
СН3СООН |
<=> |
H+ + CH3COO- |
1,76·10-5 |
|
NH4OH |
<=> |
NH4+ + OH- |
1,79·10-5 |
|
HNO2 |
<=> |
H+ + NO2- (18 °C) |
4·10-4 |
|
H2S |
<=> |
H+ + HS- |
6·10-8 |
|
H3PO4 |
<=> |
H+ + H2PO4- |
7,52·10-3 |
|
HF |
<=> |
H+ + F- |
6,61·10-4 |
|
HCN |
<=> |
H++CN- |
7,9·10-10 |
Ионообменные реакции
Реакции в растворах электролитов, при которых не происходит изменения зарядов ионов, входящих в соединения, называются ионообменными реакциями.
Правило Бертолле: равновесие в ионообменных реакциях смещается в сторону образования наименее диссоциированных соединений.
В соответствии с этим направление реакций ионного обмена определяется следующим эмпирическим правилом: ионные реакции протекают в сторону образования осадков, газов, слабых электролитов, комплексных ионов.
При написании уравнений ионных реакций сильные электролиты пишут в диссоциированном виде, слабые – в недиссоциированном.
Образование осадков:
AgNO3 + NaCl ® AgCl¯ + NaNO3
В растворе: Ag+ + NO3- + Na+ + Cl- ® AgCl¯ + Na+ + NO3-.
Исключим ионы, которые не взаимодействуют, тогда уравнение имеет вид:
Ag+ + Cl- ® AgCl¯.
Уравнения такого вида называются ионными.
Ионное уравнение получение гидроксида железа запишется следующим образом:
Fe3+ + 3OH- ® Fe(OH)3¯.
Образование газов:
Na2S + H2SO4 ® H2S + Na2SO4;
2Na+ + S2- + 2H+ + SO42- ® H2S + 2Na+ + SO42-;
2H+ + S2- ® H2S.
Образование слабых электролитов:
а. образование воды. Реакция, протекающая с образованием воды при взаимодействии ионов водорода (точнее, ионов гидроксония) и гидроксид–ионов, называется реакцией нейтрализации.
NaOH + HCl ® H2O + NaCl
OH- + H+ ® H2O
(H3O+ + OH- ® 2H2O).
в. образование слабого основания.
NH4+ + Cl- + K+ + OH- ® NH4OH + K+ + Cl-
NH4+ + OH- ® NH4OH.
с. образование слабой кислоты.
2СH3COO- + 2Na+ + 2H+ + SO42- ® 2CH3COOH + 3Na+ + SO42-
CH3COO- + H+ ® CH3COOH.
Ионное произведение воды
Процесс электролитической диссоциации воды протекает в две стадии: 1. образование водородных ионов и гидроксид–ионов:
Н2О <=> Н+ + ОН-
2. гидратация водородного иона с образованием гидроксония–иона:
Н+ + Н2О <=> Н3О+.
Первая стадия этого процесса протекает с поглощением тепла, вторая – с выделением его значительного количества. Поэтому практически все ионы водорода гидратированны и диссоциация воды должна изображаться следующим уравнением:
2Н2О <=> Н3О+ + ОН-.
При 22 оС степень электролитической диссоциации воды равна 1,8·10-9, то есть из 555000000 молекул воды диссоциирует одна. Следовательно, вода – очень слабый электролит, и для описания процесса ее диссоциации применим закон действующих масс:
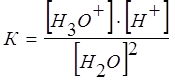 ,
,
где К - константа диссоциации воды.
[Н3О+]·[ОН-] = К·[Н2О]2
Так как [Н2О] = const, то получим:
[Н3О+][ОН-] = Кw.
Постоянная Кw называется ионным произведением воды.
В 1 л воды, массу которой можно принять равной 1000 г, находится 1000 г/18 г = 55,5 моль вещества (ее молярная концентрация).
Следовательно, при 22 °С концентрации ионов гидроксония и гидроксид–ионов равны:
[Н3О+][ОН-] = 55,5·1,8·10-9 = 1,000·10-7 г-ион/л.
Величина Кw возрастает с повышением температуры, так как при этом увеличивается степень электролитической диссоциации: ![]() . При комнатной температуре принимают округленное значение ионного произведения воды 10-14.
. При комнатной температуре принимают округленное значение ионного произведения воды 10-14.
Водородный показатель
Водные растворы различных соединений могут давать кислую, щелочную или нейтральную реакцию. Реакция среды зависит от соотношения концентраций ионов гидроксония и гидроксид–ионов в растворе.
Если концентрации этих ионов равны между собой, то есть [Н3О+] = [ОН-], то реакция среды нейтральная. Следовательно, вода принадлежит к типичным амфотерным соединениям, совмещающим кислотные и основные свойства, выраженные в одинаковой степени.
Если концентрация ионов гидроксония больше концентрации гидроксид–ионов, то есть [Н3О+] > [ОН-], то реакция среды становится кислой. Кислотность тем выше, чем больше концентрация ионов гидроксония. Если наоборот, концентрация ионов гидроксония меньше концентрации гидроксид–ионов, то есть [Н3О+] < [ОН-], то реакция среды становится щелочной. Следовательно, по значению концентрации этих ионов можно количественно охарактеризовать реакцию среды.
Кислотность или основность раствора можно выразить, взяв вместо концентрации ионов водорода ее десятичный логарифм. Чтобы избавиться от отрицательной степени в значении концентрации ионов водорода, предложено пользоваться отрицательным значением логарифма величины [Н+], названным водородным показателем или рН:
