Алифатические нитросоединения
В настоящее время установлено, что в растворе азотной кислоты в серной имеет место равновесие:
2 H2SO4 + HNO3 « NO+2 + H3O+ + 2 HSO-4
Чистая азотная кислота в условиях нитрования диссоциирует по схеме:
2 HONO2 « NO+2 + NO-3 + H2O
Сам процесс нитрования с участием нитроний-катиона NO+2 представляет собой замещение водорода:

2. Нитросоединения с нитрогруппой в боковой цепи получают теми же методами, что и нитросоединения алифатического ряда:
1. Нитрование гомологов бензола разбавленной азотной кислотой (реакция Коновалова).
Ar-CH3 + HONO2 ® Ar-CH2NO2 + H2O
Реакция галогенпроизводных с галогеном в боковой цепи с нитритом серебра (реакция Мейра)
C6H5-CH2Cl + AgNO2 ® C6H5-CH2NO2 + AgCl
Химические свойства
Химические свойства нитросоединений ароматического ряда обусловлены присутствием в молекулах нитрогруппы и ароматического ядра и их взаимного влияния.
1. Восстановление.
Впервые нитробензол был восстановлен в анилин с помощью сернистого аммония в 1842 г. Н.Н. Зининым. Это открытие сыграло важнейшую роль в развитии химической технологии, особенно в области химии красителей, медикаментов и фотохимикатов. Ароматические нитросоединения в зависимости от условий восстановления дают различные продукты. Ароматические амины являются конечными продуктами восстановления. Обычно их получают в кислой среде.
В нейтральной, щелочной и слабокислой средах можно получить различные промежуточные продукты восстановления. Ниже приведена схема восстановления нитросоединений:
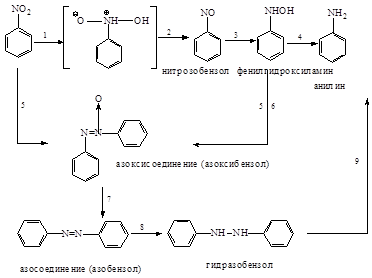
В нейтральной и кислой средах идут реакции 1-4, причем в кислой среде не удается выделить промежуточные продукты. В нейтральной среде можно выделить нитрозобензол и фенилгидроксиламин. В щелочной среде нитро- и нитрозобензолы конденсируются с фенилгидразином и идут реакции 5-9. Различные продукты восстановления можно получать, пользуясь методом электролитического восстановления. В зависимости от потенциала на электродах можно получать различные вещества.
2. Реакции замещения.
Нитрогруппа в реакциях электрофильного замещения направляет заместитель в мета-положение причем реакционная способность бензольного кольца уменьшается:

В реакциях нуклеофильного замещения нитрогруппа направляет заместители в орто- и пара-положения. Так, при нагревании нитробензола с порошкообразным KOH получается смесь о- и п-нитрофенолятов:

Благодаря сильно выраженному электроноакцепторному характеру нитрогруппа оказывает значительное влияние на атомы и группы, находящиеся по отношению к ней в о- и п-положениях. Так, в случае о- и п-нитрохлорбензолов галоген под влиянием нитрогруппы приобретает высокую подвижность, и легко замещается на гидроксил, алкоксил или аминогруппу:

