Сравнительная характеристика химического состава и пищевой ценности тропических плодов
Если определяют аскорбиновую кислоту в темноокрашенных растворах, то рядом ставят третью колбу для сравнения окраски. Даже в интенсивно розовых растворах ясно проявляется фиолетовая окраска, появляющаяся от одной капли йода с крахмалом.
1см 0,001н раствора йодида калия соответствует 0,088 мг аскорбиновой кислоты. Раствор йодида калия удобно приготовить из фиксонала, получая сначала 0,1н раствор, из которого по мере надобности приготавливают 0,001н раствор.
Одним из преимуществ раствора йодида калия взамен 2,6 - дихлорфенолиндофенола является его устойчивость. Кроме того, нет необходимости ежедневно проверять титр, как это требуется для раствора краски 2,6 – дихлорфенолиндофенола.
Содержание аскорбиновой кислоты рассчитывают по формуле:
X = (V*T*M*V1*100) / A*V2,
где
V – количество 0,001н раствора йодида калия, израсходованного на титрование вытяжки, см3;
Т – 0,088 мг аскорбиновой кислоты, соответствующей 1 см3 0,001н раствора йодида калия;
V1 - общий объем водной вытяжки, см3;
100 – пересчет в мг %;
А – навеска исследуемого продукта, г;
V2 – объем вытяжки, взятой для титрования, см3.
Определение витамина В2 люминофвоавиновым методом.
Проводят в соответствии с ГОСТ 25999 – 83.
В колбу вместимостью 250 см3 помещают 100 см3 анализируемого гидролизата, в другую – 100 см3 контрольного опыта. В обе колбы прибавляют по 2 см3 раствора серной кислоты. Затем пипеткой с делениями по каплям при постоянном перемешивании прибавляют раствор марганцовокислого калия до слабо-розового окрашивания, не исчезающую в течении одной минуты. Избыток розового окрашивания устраняют прибавлением по каплям раствора перекиси водорода. Отмечают израсходованные объемы растворов марганцовки и перекиси водорода. Полученный раствор переносят в делительную воронку вместимостью 250 см3, прибавляют 30 – 50 см3 хлороформа и встряхивают 0,5 мин. Хлороформный слой удаляют, а водный экстракт используют для анализа.
Облучение экстракта и получение люминофлавина.
В две колбы вместимостью 100 см3 каждая прибавляют по 20,0 см3 анализируемого экстракта, в третью – экстракт контрольного опыта. В колбу с анализируемым экстрактом прибавляют 2,0 см3 стандартного раствора рибофлавина с массовой концентрацией 0,001 г/л и затем во все колбы по 4,0 см3 раствора гидроксида натрия с молярной концентрацией с NaOH = 1 моль/л. Содержимое перемешивают, колбы закрывают пришлифованными пробками и облучают светом электролампы мощностью 100 – 200 Вт с расстояния 30 см в течении 40 мин.
Температура раствора должна быть от 15 до 25 0С. После облучения в колбы прибавляют по 4,0 см3 ледяной уксусной кислоты, перемешивают, прибавляют по 20,0 см3 хлороформа и снова перемешивают в течении 0,5 мин. Содержимое колб переносят в делительные воронки вместимостью 50 см3 и после расслаивания хлороформный раствор фильтруют в кюветы для измерения интенсивности флуоресценции. Для обезвоживания хлороформного раствора на воронке с фильтратом помещают около 2,5 г безводного сернокислого натрия.
После этого измеряют интенсивность флуоресценции сначала раствора с добавкой рибофлавина, затем без добавки и контрольного опыта.
Массовую долю витамина В2 в процентах определяют по формуле
X = [(А – А1) – (С – С1)]*b*V*100 / [(Д – Д1) – (А – А1)]*V1*m,
где
А – интенсивность флуоресценции раствора анализируемой пробы до прибавления гидросульфата натрия;
А1 – интенсивность флуоресценции раствора анализируемой пробы после прибавления гидросульфата натрия;
С – интенсивность флуоресценции раствора контрольного опыта до прибавления гидросульфата натрия;
С1 – интенсивность флуоресценции раствора контрольного опыта после прибавления гидросульфата натрия;
Д – интенсивность флуоресценции раствора анализируемой пробы добавкой рибофлавина до прибавления гидросульфата натрия;
Д1 – интенсивность флуоресценции раствора анализируемой пробы с добавкой рибофлавина после прибавления гидросульфата натрия;
b – масса рибофлавина в стандартном растворе рибофлавина, добавленной в гидролизат анализируемой пробы, г;
V – общий объем гидролизата, см3;
V1 – объем гидролизата, взятый для окисления, см3;
m – масса навески продукта, г.
За окончательный результат принимают среднее арифметическое двух последних определений.
Расчет данных физико-химических показателей качества тропических плодов приведен в приложении 4
3.4 Определение интегрального показателя конкурентоспособности тропических плодов
При контроле качества товаров обычно учитывают базовые показатели, т. е. Показатели, принятые за исходную (эталонную) величину. Применительно к пищевым продуктам в качестве базовых показателей используют требования, которые содержатся в нормативных документах. Однако каждый отдельно взятый базовый показатель характеризует лишь одно из свойств товара. Всесторонняя, комплексная оценка качества товаров может быть получена с помощью интегрального показателя.
Интегральный показатель качества отражает показатели полезности и розничной (или оптовой) цены на товар. При разработке формулы учитывается следующее: число аналогичных товаров на потребительском рынке, среднюю цену аналогичного товара, цену изучаемого товара, содержания белков, жиров, углеводов, калорийность изучаемого товара, приведенного в маркировке согласно указанного в нем стандарта и рекомендуемое или среднее содержание основных пищевых веществ и калорийность в аналогичных товарах.
Интегральный показатель качества выражается отношением качества товара к цене по формуле:
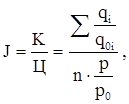 (1)
(1)
где
n – число сравниваемых характеристик;
qi – содержание I-го вещества в изучаемом продукте, г в 100 г продукта;
q0i – среднее содержание I – го вещества в аналогичных товарах, г в 100 г продукта;
p – цена 100 г изучаемого товара, руб.;
p0 – средняя цена 100 г аналогичного товара.
Смещение значения интегрального показателя в сторону качества, т. е. Когда J>1, свидетельствует либо о применении предприятием агрессивной стратегии в стремлении завоевать большую часть рынка за счет использования заведомо низких цен, либо о неэффективной ценовой стратегии, в результате которой предприятие теряет честь прибыли.
Смещение значения показателя в сторону цены, т. е. Когда J<1, характеризует ситуацию престижного ценообразования для товаров с низкими показателями качества.
Рассчитаем интегральный показатель качества для тропических плодов.
Основные данные, необходимые для расчета, представлены в таблице 10.
Таблица 10. Данные для расчета интегрального показателя качества.
|
Наименование плода |
Химический состав, на 100г продукта |
Цена 100 г продукта, руб. | |||
|
Белки (г) |
Углеводы (г) |
Минеральные вещества (мг) |
Витамины (мг) | ||
|
Бананы |
1,5 |
21,0 |
457,6 |
10,81 |
3,82 |
|
Ананасы |
0,4 |
11,5 |
380,3 |
20,35 |
5,91 |
|
Манго |
0,6 |
15 |
500 |
183 |
9,89 |
|
Авокадо |
2 |
6 |
658,4 |
11,4 |
8,93 |
