Платина и рак - биохимия, физиология, медицина
В итоге, несмотря на высокую эффективность подавления роста опухолей препаратами платины, такая терапия обходится организму очень и очень дорого. Вопрос при лечении развитых опухолей перед пациентом обычно ставится так: умереть через несколько месяцев от рака или через пять-шесть лет от последствий его терапии. Третьего, к сожалению, пока не дано, но интенсивные поиски более эффективных и менее токсичных лекарств сейчас ведутся в сотнях лабораторий по всему миру.
ЛЕКАРСТВА
В заключение будет дана сводка наиболее перспективных в настоящее время препаратов платины – так называемых препаратов второго поколения, обладающих улучшенными показателями противоопухолевой активности и токсичности по сравнению с цисплатином.[8] Структурные формулы приведены в Приложении 1.
Карбоплатин (синонимы CBDCA, JM-8).
Место синтеза: Великобритания
Диапазон оптимальных доз: 20-25 мг/кг
Спектр действия: мелко- и немелкоклеточный рак легкого, яичников, почки, толстой и прямой кишки, молочной железы, семинома, меланома, саркома мягких тканей, опухоли головы и шеи, рак эндометрия, рак щитовидной железы, мезотелиома плевры.
Основные побочные эффекты: гематотоксичность, аплазия лимфоидной ткани, атрофия половых желез, повреждение эпителия кишечника.
Достоинства: малая нефротоксичность, растворимость в воде (в 5 раз выше ДДП).
DACCP(синоним: JM-82).
Место синтеза: США
Диапазон оптимальных доз: 600-800 мг/м2
Спектр действия: рак легкого, желудка, шейки матки, назофарингеальной области.
Основные побочные эффекты: миелодепрессия, тромбо- и лейкопения, атрофия лимфатических узлов.
Достоинства: токсичность в 8-10 раз ниже ДДП, хорошо растворим в растворе гидрокарбоната.
Спироплатин (синоним: TNO-6).
Место синтеза: США и Нидерланды
Диапазон оптимальных доз: 30 мг/м2
Спектр действия: рак молочной железы, аденокарцинома легкого.
Основные побочные эффекты: миелодепрессия, нефротоксичность, электролитные нарушения состава крови, затруднение слюноотделения, потеря вкуса.
Достоинства: отсутствие перекрестной устойчивости с ДДП, хорошая растворимость в воде.
Недостатки: нестабилен в физрастворе, высоко токсичен.
PHIC.
Место синтеза: Франция
Диапазон оптимальных доз: ~100 мг/кг
Спектр действия: не сообщается.
Основные побочные эффекты: не сообщается.
Достоинства: отлично растворим в воде, не имеет перекрестной устойчивости с ДДП, не обладает ни нефро-, ни гематотоксичностью, быстро распространяется по органам и тканям.
Недостаток: так что же он все-таки лечит?
PYP.
Место синтеза: не сообщается.
Диапазон оптимальных доз: 10-30 мг/м2
Спектр действия: лейкоз, меланома, аденокарцинома молочной железы.
Основные побочные эффекты: аплазия костного мозга, тошнота, рвота, диарея.
Достоинства: хорошо растворим в воде, обладает аддитивным действием с ДДП.
Недостаток: нестабилен в физрастворе.
Циклоплатам.
Место синтеза: СССР.
Диапазон оптимальных доз: 10-25 мг/м2
Спектр действия: “имеет значительную терапевтическую широту” (цитата).
Основные побочные эффекты: не сообщается.
Достоинства: хорошо растворим в воде, не проявляет нефротоксичности, не имеет перекрестной устойчивости с ДДП.
Недостаток: у советских препаратов недостатков нет! J
Ипроплатин (синонимы: CHIP,JM-9).
Место синтеза: США.
Диапазон оптимальных доз: 100-200 мг/м2
Спектр действия: не сообщается.
Основные побочные эффекты: аплазия костного мозга, повреждение лимфоидной ткани, повреждение желудочно-кишечного тракта, тошнота, рвота, гипотензия.
Достоинства: не проявляет нефротоксичности, хорошо растворим в воде.
Оксоплатин.
Место синтеза: СССР.
Диапазон оптимальных доз: не сообщается
Спектр действия: “широкий” (цитата)
Основные побочные эффекты: не сообщается
Достоинства: обладает сильным антиметастатическим действием, не проявляет нефротоксичности.
Недостаток: плохо растворим в воде.
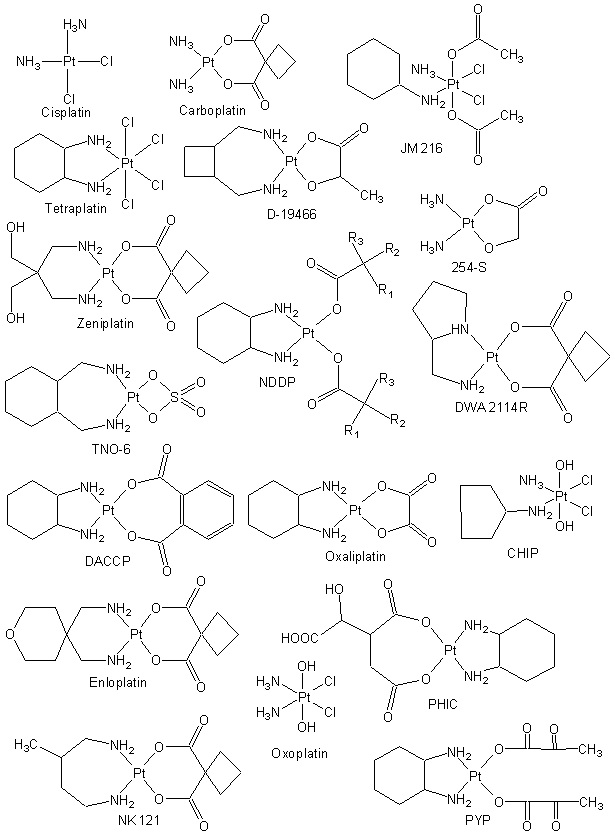 Приложение 1. Клинически используемые противораковые комплексы платины.[9]
Приложение 1. Клинически используемые противораковые комплексы платины.[9]
ЛИТЕРАТУРА
* Традиционная активность – “токсично” – была известна и до нашей эры.
* Впрочем, разного рода “целители” иногда изготовляют платиновые талисманы, но злые духи в списке известных патогенов пока не значатся.
* Что конкретно происходит с платиновыми препаратами в кровяном русле, не ясно до сих пор.
* И токсичность его существенно ниже.
** Боевое отравляющее средство, впервые применено Германией против англо-французских войск в первую мировую войну возле бельгийского местечка Ипр.
* В организм человека ДДП вводится внутривенно.
** Практически любой белок содержит серу в виде свободных SH-групп или дисульфидных S-S-мостиков.
* Современное объяснение нервной токсичности препаратов платины базируется именно на факте нарушения работы ферментов. На транскрипцию и биосинтез белка (нормальными ферментами) воздействия обнаружено не было. Делиться же нервным клеткам не требуется.
** Радикальное окисление перекисями, алкилирование уже упомянутыми “горчицами”, метилирование и т.д.
[1] И.В. Петрянов-Соколов (ред.) // Популярная библиотека химических элементов. // Москва, Наука, 1983 г.
[2] J. Reedijk // The mechanism of action of platinum anti-tumor drugs. // Pure & Applied Chemistry, 1987, vol. 59, № 2, pp. 181-192.
[3] J.J. Roberts, A.J. Thomson // The mechanism of action of antitumor platinum compounds. // Progress in Nucleic Acid Research and Molecular Biology, 1979, vol. 22, pp. 71-133
[4] B. Lippert // Impact of Cisplatin on the recent development of Pt coordination chemistry: a case study. // Coordination Chemistry Reviews, 1999, 182, pp. 263-295
[5] В.А. Филов (ред.) // Вредные химические вещества. Неорганические соединения элементов V-VII групп. // Ленинград, Химия, 1989.
[6] J. Reedijk // The relevance of hydrogen bonding in the mechanism of action of platinum antitumor drugs. // Inorganica Chimica Acta, 1992, vol. 198-200, pp.873-881.
[7] A. Pasini, F. Zunino // New cisplatin analogues – on the way to better antitumor drugs. // Angewandte Chemie International Edition English, 1987, 26, pp. 615-624.
[8] М.А. Преснов, А.Л. Коновалова, В.А. Горбунова // Второе поколение противоопухолевых комплексных соединений платины в экспериментальной к клинической практике. // Вестник Академии Медицинских Наук СССР, 1986, 12, pp. 79-89.
[9] L.R. Kelland, S.J. Clarke, M.J. McKeage // Advances in platinum complex cancer chemotherapy. // Platinum Metals Reviews, 1992, 36, 4, 178-184.
