Страница
2
Но аналогичным способом можно картировать и интроны. Для них маркерами обычно служат так называемые сайты узнавания. Дело в том, что существуют специальные ферменты, предназначенные для разрезания ДНК, - рестриктазы. Это белковые молекулы особого устройства. Грубо говоря, они попросту "шинкуют" ДНК, режут на отрезки, но не как попало, а в определенных местах. Всякая рестриктаза может опознать лишь одну стандартную последовательность из нескольких нуклеотидов. Последняя и становится сайтом узнавания для фермента. А уж как тот "покромсает" ДНК, зависит от того, сколь густо она "усеяна" сайтами узнавания. Молекулы рестриктазы химически связываются с ними и в этих местах рвут цепь ДНК.
Имеются сравнительно простые методы измерения длин участков, на которые порезала молекулу ДНК рестриктаза. Любое изменение сайта узнавания ведет к тому, что тот становится "невидимым" для фермента. А значит, ДНК разрезается в других местах и образуются иные по длине фрагменты.
Чем хорош метод картирования по генетическому сцеплению – его можно применять, не имея ни малейшего представления о структуре генов тех или иных признаков. Достаточно уверенности, что таковые гены есть, а дальнейшие мероприятия направлены на то, чтобы узнать, ГДЕ они, а не КАКИЕ они.
Недостатки метода – довольно низкая разрешающая способность (7-10 Мб) и высокая трудоемкость. Кроме того, ген на карте предстает не протяженным отрезком ДНК (каков он "на местности"), а точкой на линии, изображающей ее двойную цепь.
Наконец, к великому сожалению, человек – не дрозофила. Очень легко считать частоту рекомбинации маркеров, скрещивая мелких мушек тысячами и десятками тысяч. А с Homo sapiens такой способ по понятным причинам не годится, и о частоте рекомбинации приходится судить по статистическим данным – скажем, по заболеваемости таким-то наследственным недугом в стольких-то семьях за столько-то десятилетий (а то и веков). Кстати, именно генетическое картирование помогло найти точное расположение на хромосомах генов многих тяжелых наследственных болезней – муковисцидоза, серповидно-клеточной анемии, хореи Гентингтона, болезни Тея-Сакса, поликистоза почек, миотонической дистрофии и других.
Мелкомасштабные физические карты
К ним относят хромосомные и карты кДНК ("к" значит "кодирующей").
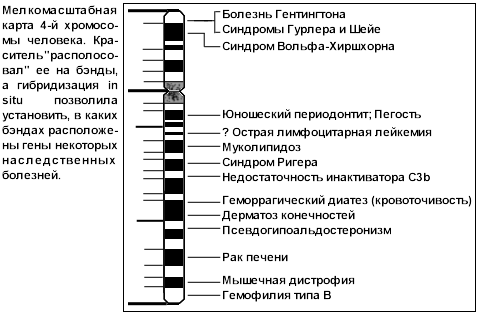
Хромосомное картирование довольно грубо, но имеет смысл, когда нужный ген держат, что называется, в руках: известна его структура, он химически выделен, но неизвестно, где он "сидит". Тогда хромосомы, извлеченные из ядра клетки во время ее деления (когда они толстые и хорошо различимы), обрабатывают особыми красителями, придающими им "полосатость": получаются так называемые бэнды – разноокрашенные участки хромосом. Искомый ген размножают в пробирке и при этом метят его копии, подменяя, например, водород тритием. За таким радиоактивным зондом очень удобно следить: если подмешать его к препарату хромосом и выдержать некоторое время, он химически свяжется с определенным бэндом определенной хромосомы, встав "на свое место" (это называется "гибридизация in situ", т.е. "на месте"). Так были картированы гены альбумина, коллагена, гормона роста и некоторые другие.
Средний размер бэнда – около 10 Мб: такова и точность хромосомной карты. Правда, позднейшее усовершенствование – гибридизация с флуоресцентной меткой (FISH – fluorescent in situ hybridization) – повысило разрешение до 5-2 Мб. Более того, разработан даже метод гибридизации меченых генов с хромосомами, извлеченными из ядра неделящейся клетки – и значит, де конденсированными, "развинченными", а не упакованными в компактные образования. В итоге удалось локализовать участки до 0,1 Мб.
 |
Крупномасштабные карты генома
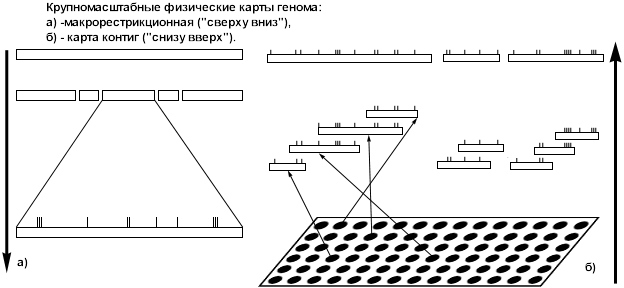
Их составляют по общему принципу: сначала кромсают ДНК на куски, разгоняют получившиеся фрагменты в электрическом поле (электрофорез) и затем гибридизируют с меченым зондом. В результате фрагменты упорядочиваются – воссоздается их исходная последовательность. Для этого используют разные методы поиска перекрывающихся участков.
В любом случае необходимо прежде всего получить фрагменты ДНК картируемого участка в больших количествах. ДНК размножают обычно двумя способами – клонированием и ПЦР.
КЛОНИРОВАНИЕ – по современным понятиям сравнительно примитивный метод. Последовательность действий такова: порезали рестриктазой изучаемый участок ДНК – вставили каждый ее отрезок в молекулу вектора (бактериальной, дрожжевой или другой кольцевой ДНК), разрезанную в одной точке той же рестриктазой: получилась рекомбинантная кольцевая ДНК с "чужой" вставкой. Такую смешанную ДНК "вселяют" в ядро клетки-хозяина (обычно бактерии), и та принимается делиться в культуре, благодаря рекомбинантная ДНК – и.о. ее генома – размножается практически до любого количества копий. Результат – набор клонов разных фрагментов картируемой ДНК, или, как его обычно называют, библиотека клонов.
ПОЛИМЕРАЗНАЯ ЦЕПНАЯ РЕАКЦИЯ (ПЦР) – лабораторный синтез фрагментов ДНК без клетки-хозяина. В пробирку к фрагменту, который надо размножить, "подсаживают":
а) фермент ДНК-полимеразу, который осуществляет воспроизведение ДНК в живых клетках;
б) стройматериал, т.е. отдельные нуклеотиды;
 |
Затем пробирку нагревают – фрагмент от жары "расклеивается", разделяясь на две цепи; пробирку охлаждают – праймеры присоединяются к концам фрагмента и полимераза начинает свое дело. Чередуя нагревания и охлаждения, можно за полтора часа довести количество копий нужного участка ДНК до нескольких миллионов – в чем и состоит главное преимущество ПЦР перед клонированием. Но у нее есть два недостатка. Один уже упомянут – нужно знать праймеры "в лицо", иначе реакцию не удастся запустить. Второй – техническая невозможность копировать фрагменты длиннее 5-6 п.н.
