Прыжки по хромосоме
11. Препаративные гели для определения размеров ДНК можно готовить из легкоплавкой агарозы. И тогда выделять ДНК из них можно, вырезая нужные участки и расплавляя их при 65°С. После того как гель расплавится, ДНК доводят до нужной концентрации и проводят лигирование в присутствии агарозы, которая не ингибирует эту реакцию. В настоящее время нет оснований предпочитать один метод другому. Важно лишь избегать операций, которые могли бы нарушить целостность молекул ДНК после извлечения их из геля. Нельзя центрифугировать, встряхивать, пипетировать препараты. И желательно как можно скорее приступать к их лигированию.
2.4 Циклизация
Успех или неудача «прыжков по хромосоме» в решающей степени определяются возможностью лигировать большие сегменты ДНК с образованием кольцевых молекул. Анализ стратегии этого метода, схематически изображенной на рис. 4, показывает, что тандемное лигирование молекул ДНК дает сцепленные фрагменты, соединяющие в себе две случайные последовательности. Такое сцепление приводит к образованию аномальных клонов, которые провоцируют «прыжки по хромосоме» из данной стартовой точки на какую-то случайную последовательность генома. Свести к минимуму риск возникновения такого события можно, проводя лигирование при достаточно низких концентрациях ДНК так, чтобы на долю тандемных лигирований приходилось менее 5–10%.
Теория лигирования ДНК при низких концентрациях была разработана в 50-е годы Джекобсоном и Стокмайером. Для некоторых размеров последовательностей ДНК теоретические прогнозы подтвердились экспериментально. Очень полезно, например, следующее соотношение:
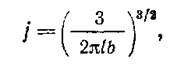
где j – концентрация молекул ДНК контурной длины / и сегментной длины b, при которой с равной вероятностью лигируются как разные молекулы, так и концы одной молекулы. Очевидно, что для эффективной циклизации лучше работать с концентрациями гораздо более низкими, чем /. Подставляя в уравнение известные параметры ДНК для водного раствора, его можно преобразовать следующим образом:
![]()
где т.п.н. – длина ДНК в тысячах пар нуклеотидов. При данной концентрации ДНК i – доля лигирований, приводящих к циклизации. Чтобы эта доля достигала 90%, работать следует с концентрацией ДНК, определяемой уравнением:
![]()
Обычно для получения 3х106 клонов в библиотеке, необходимо после расщепления циклизованных молекул ДНК иметь 0,5 мкг сцепленных фрагментов. Средний размер такого фрагмента 5 т. п.н., а это значит, что для осуществления прыжков в 100 т. п.н. необходимо иметь 10 мкг фракционированной по размеру ДНК; для прыжков в 200 т. п.н. – уже 20 мкг. На интенсивность лигирования влияют два фактора: 1) количество ДНК, необходимое для получения достаточного числа сцепленных фрагментов и создания геномной библиотеки. Это количество возрастает линейно с увеличением размера прыжка; 2) необходимость преимущественного получения циклизованных молекул. Интенсивность лигирования с циклизацией возрастает пропорционально квадратному корню длины молекул ДНК. Поэтому с увеличением размера прыжка объем лигазной смеси должен возрастать пропорционально 3/2 степени длины молекулы ДНК. В табл. 1 приведены стандартные параметры для создания геномной библиотеки, рассчитанной на прыжки в 100 т. п.н.
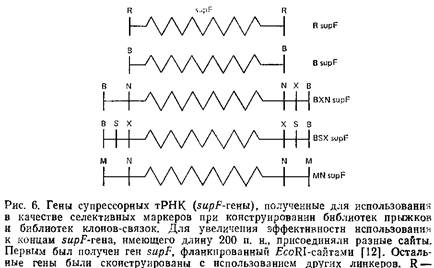
Очень важно маркировать в кольцевых молекулах места соединения фрагментов с тем, чтобы селективно клонировать их на последующих стадиях. В качестве селективного маркера мы использовали ген супрессорной тРНК – supF, хотя возможны и другие способы селекции. Супрессорный ген должен иметь концы, комплементарные Mfeol-концевым фрагментам геномной ДНК – Для этой цели было взято несколько supF с различающимися концевыми последовательностями, полученными при обработке рестриктазной Ват.
Ниже представлена методика реакции циклизации.
1. Используя приведенные выше уравнения, растворите ДНК и доведите раствор до нужной концентрации в 50 мМ Трис, рН 7,4, 1 мМЭДТА.
2. Добавьте 100 или 500-кратный молярный избыток ДНК BamHI-фрагмёнтов supF, предварительно проверенных на эффективность лигирования. Для этого проведите самолигирование и последующий анализ геля. По нашему мнению, наиболее удобно получать фрагменты генов supF электрофорезом с последующей электроэлюцией. Важно, чтобы фрагмент был максимально очищен от плазмиды, поскольку даже незначительные количества ее могут проявиться в окончательной библиотеке в виде клонов, гибридизующихся с зондом, несущим плазмиду. Оставьте смесь supF ДНК с геномной ДНК на полчаса.
3. Доведите концентрацию магния до 10 мМ и оставьте смесь еще на 10 мин, чтобы установилось равновесие. Затем добавьте ДНК-лигазу бактериофага Т4 до конечной концентрации 1–2 ед./мкл. Лигируйте 12 ч при 14°С, затем добавьте вторую порцию лигазы и лигируйте еще 12 ч. Осадите циклизовавшуюся ДНК этанолом, добавив 20 мкг дрожжевой тРНК-носителя. Отцентрифугируйте осадок при 23000 об/мин в роторе SW27. Ресуспендируйте осадок в 100 мкл ТЕ и инактивируйте все нелигировавшиеся концы, либо обработав их щелочной фосфатазой, либо добавив фрагмент Клёнова ДНК-полимеразы I. Эта стадия очень важна, так как, если лигирование при низких концентрациях происходит не полностью, свободные фрагменты могут аномально лигироваться с вектором. Экстрагируйте ДНК фенолом, осадите и, растворив, снова обработайте EcoRl.
5. Для контроля очень полезно на каждой стадии отбирать небольшие аликвоты и подвергать их электрофорезу в 1,4%-ном агарозном геле с последующим переносом на нитроцеллюлозу или полиамид и блот-гибридизацией с supF-гтом. В случае успешной реакции циклического лигирования ДНК гена supF будет давать полосы в виде лестницы, и небольшое ее количество должно оказаться в той зоне геля, которая соответствует высокомолекулярной ДНК. После обработки рестриктазой ЕсоЩ лесенка supF-гена должна остаться, а полосы из высокомолекулярной области должны расщепиться на множество фрагментов размером от 1 до 20 т. п.н.
6. ДНК, обработанную ЕсоШ, экстрагируйте фенолом и осадите этанолом.
2.5 Клонирование и скрининг
На этой стадии обработанные кольцевые молекулы геномной ДНК уже можно лигировать и производить селекцию сцепленных фрагментов. Для селекции геномные фрагменты встраивают в фаговый вектор, несущий амбермутации по крайней мере двух генов белковой оболочки, упаковывают фаговую ДНК in vitro и инфицируют клетки бактерии-хозяина, лишенные функции supF. Формировать бляшки на таком газоне могут только те фаговые частицы, геномы которых содержат собственные supF-гены.
Теоретически подходит любой фаговый вектор, несущий амбер-мутации и клонирующий сайт. Желательно, конечно, чтобы этот вектор обеспечивал максимальную клонирующую емкость. Идеальной можно считать ситуацию, когда кольцевые геномные фрагменты расщеплялись бы лишь частично мелкощепящим ферментом, а затем лигировались в вектор большой емкости, чтобы не было дискриминации фрагментов, обусловленной расположением сайтов рестрикции. Однако обязательные потери, происходящие при частичном расщеплении, оказываются препятствием на пути создания полной библиотеки. Имеющиеся у нас в настоящее время стандартные геномные библиотеки для «прыжков по хромосоме» были получены в результате полного расщепления кольцевых геномных фрагментов рестриктазой EcoRl. Можно использовать и другие ферменты, для которых имеются амбермутантные фаговые клонирующие векторы.
