Простейшие бифункциональные природные соединения - мостик к массиву природных соединений
Особые, в какой-то мере, специфические свойства проявляют оксикислоты, являющиеся интермедиатами различных биосинтетических реакций при ферментативном катализе in vivo.
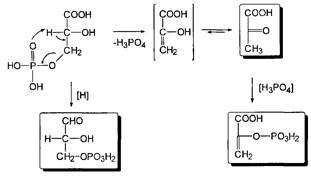
Глицериновая кислота в этих условиях обычно фигурирует в виде 3-фосфата, т.е. она избирательно этерифицируется фосфорсодержащими реагентами в присутствии ферментов по первой спиртовой группе. На следующем этапе 3-фосфат глицериновой кислоты элиминирует фрагмент фосфорной кислоты, образуя а-гидрокси-акриловую кислоту, которая сразу же изомеризуется в пировиноградную кислоту.

Но этот последний процесс является обратимым, и в условиях кислотно-основного катализа доля непредельной гидроксикислоты может быть существенной, хотя термодинамически более стабильна в данном случае б-кетокислота В свою очередь, енольная форма этой кислоты может быть стабилизирована, зафиксирована реакцией ее этерифика-ции фосфорной кислотой Таким образом, глицериновая кислота является источником двух новых соединений кислотного типа, а если учесть еще реакцию восстановления карбоксильной группы до альдегидной, то уже трех веществ, которые известны ка к важные промежуточные продукты основных химических процессов in vivo. Следует заметить, что в заметных количествах они в организмах не накапливаются.
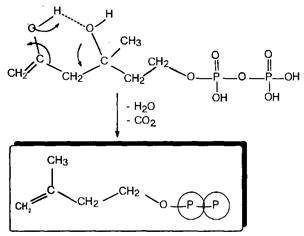
Из природных оксикислот можно выделить мевалоновую, являющуюся ключевым соединением биосинтеза изопре-ноидов, легко претерпевающую in vivo синхронное элиминирование фрагментов С02 и Н20, образуя при этом пирофосфатное производное 2-метил-бутенола, с которого и начинаются процессы формирования изопреноидных углеродных систем.
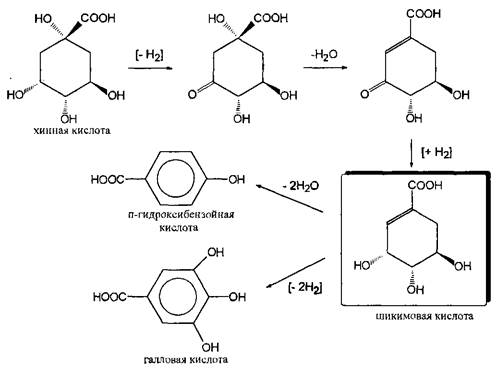
Хинная кислота, являясь исходным соединением биосинтеза ароматических кислородсодержащих соединений, может накапливаться в некоторых растениях в заметных количествах. Но основное предназначение этой кислоты — образование шикимо-вой кислоты, ключевого интермедиа-та вышеуказанных синтезов, с последующим переходом к бензольным производным, используя реакции дегидратации и дегидрогенизации.
2. Оксокислоты
Оксокислоты в природе распространены значительно меньше, чем гидроксикислоты, они редко встречаются в свободном состоянии, не накапливаются в организмах, хотя и образуются на различных стадиях биосинтеза. По поводу последнего факта нужно отметить, что в биосинтезе они играют зачастую важнейшую роль, являясь ключевыми соединениями ряда биосинтезов.
Классифицируют оксокарбоновые кислоты, как и все бифункциональные соединения, согласно взаимному расположению функциональных групп, подразделяя их при этом на альдегидо- и кетонокислоты. Многие оксокислоты носят тривиальные названия.
В структурном плане оксокислоты несколько более примитивны, чем оксикислоты — сказывается потеря асимметрического центра при переходе от гидроксикислот к оксокислотам. Так, при окислении любой формы молочной кислоты мы получим одну единственную пировиноградную кислоту. Но в тоже время, этот класс бифункциональных соединений отличается большим разнообразием химических реакций, химических особенностей, обязанных взаимному влиянию карбонильной и карбоксильной групп.
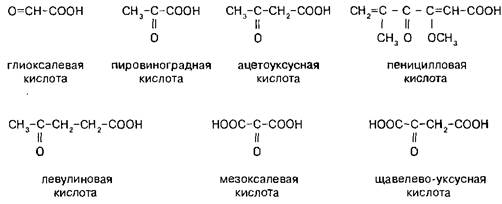
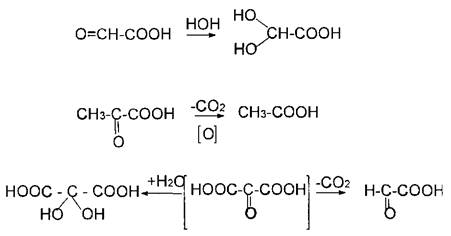
В случае б-оксокислот можно отметить легкость присоединения нуклео-фильных реагентов по карбонильной группе и легкость реакций декарбоксилирова-ния — пировиноградная кислота в условиях окислительного ферментатив-но катализируемого декарбоксилиро-вания образует уксусную кислоту. Мезоксалевая кислота сочетает в себе легкость протекания обоих этих процессов — она существует только в виде гидратированного аддукта и в водном растворе легко разлагается на глиоксалевую кислоту и двуокись углерода.
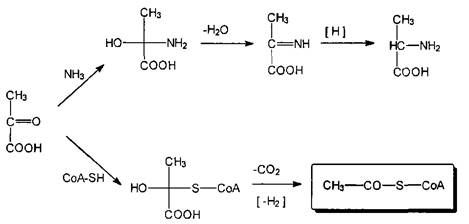
Пировиноградную кислоту следует выделить из всех б-оксокислот еще и как источник весьма существенных биологически активных соединений, получаемых in vivo в результате реакции нуклеофильного присоединения по карбонильной группе и последующих преобразований. С таким реагентом как аммиак, она в несколько стадий, включая еще реакции дегидратации и восстановления, образует важную б-аминокислоту аланин; а при взаимодействии с тиолом ферментной природы, коферментом-А, через стадии присоединения, декарбоксили-рования и восстановления, образует ацетилированный кофермент-А — важнейший интермедиат многих биосинтетических реакций.
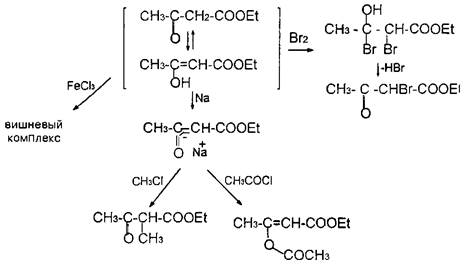
В случае в-кетокислот, на примере ацетоуксусного эфира, мы наблюдаем интереснейшее явление двойственной реакционной способности, называемое таутомерией. Применительно к указанному классу соединений, это явление названо кето-енольной таутомерией. Суть данного явления заключается в следующем: карбонильная и карбоксильная функции, будучи сильными электроноакцепторами, оголяют протоны метиленовой группы, расположенной между ними, что делает их кислыми. В силу этого водород в виде катиона может мигрировать к карбонильному кислороду несущему на себе избыточную электронную плотность; синхронно этому переходу электронная плотность карбонильной группы и у-связей метиленового фрагмента перераспределяется так, как это указано на схеме 2.2.4, образуя систему енола
Процесс является обратимым, поскольку гидроксил при тригональном углероде всегда достаточно кислый и его протон может осуществлять, в свою очередь, электрофильную атаку по С=С связи. Оба эти процесса совершаются столь медленно, что тау-томеры могут быть разделены либо кристаллизацией, либо фракционной перегонкой Но через некоторое время индивидуальные изомеры при стоянии снова превращаются в равновесную смесь соединений кетонной и енольной структуры Таким образом, ацетоуксусный эфир, кроме свойств кетонов и сложных эфиров, обнаруживает еще свойства непредельных соединений, спиртов и фенолов, так как гидроксил при двойной связи ведет себя так же, как и при ароматическом кольце
Следует отметить, что кето-енольная таутомерия проявляется и в свойствах вышеописанной пировиноградной кислоты, и хотя доля енольной формы у нее незначительна, в реакциях она реализуется часто как основная.
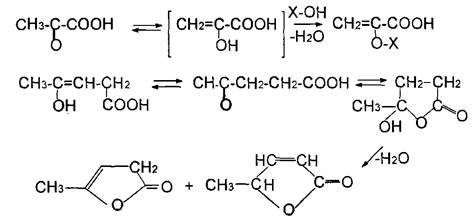
Для г- и д- оксокислот характерны как кето-енольная, так и кольчато-цеп-ная таутомерия. Результатом последней, в случае левулиновой кислоты, является гидроксилактон, наиболее устойчивая таутомерная форма этого соединения, которая достаточно легко отщепляет воду в присутствии водоот-нимающих агентов, образуя непредельные г-лактоны.
3. Аминоспирты
Алифатические соединения, содержащие амино- и гидрокси- группы, называемые аминоспиртами, классифицируют согласно взаимному расположению этих функциональных групп. 1,1-Аминоспирты — соединения достаточно нестабильные, не встречающиеся в природе, имеют значение как промежуточные в различных органических реакциях. Для химии природных соединений определенное значение имеют 1,2-аминоспирты, среди которых наибольшее значение имеет в-этаноламин, встречающийся достаточно часто в виде производных в связанном виде.
