Получение рекомбинантного аденовируса CELO
Рестриктазы являются высокоспецифическими ферментами. Однако для поддержания этой специфичности in vitro необходимо соблюдать в реакционной смеси оптимальные условия для действия ферментов. При нарушении таких условий у некоторых рестриктаз начинает проявляться вторичная (так называемая штриховая) активность. Так, рестриктаза EcoRI расщепляет последовательность GAATTC при рН 7,3, 100 мМ NaCl в присутствии 5 мМ MgC12, однако при изменении значений рН, понижении концентрации NaCl или замене ионов Mg2+ на Мп2+, а также в присутствии органических растворителей у фермента появляется тенденция к расщеплению более короткой последовательности ААТТ (так называемая активность EcoRI). К рестриктазам, обладающим подобными свойствами, относятся также BamHI, BstI, Bsul, Ddel, Hhal, PstI, Sail, SstI, Xbal.
В природе существуют антагонисты рестриктаз - метилазы. Это ферменты, которые катализируют реакции метилирования А или Ц в немногих специфических сайтах в хромосомах, в результате чего метилированная ДНК оказывается нечувствительной к атакам рестриктазами. Метилазы используются для ограничения числа сайтов рестрикции и получения более крупных фрагментов ДНК с помощью рестриктаз.
Большинство штаммов Е. coli содержит два типа ферментов, метилирующих ДНК: dam- и dcm-метилазы. Первая осуществляет перенос метальных групп в N-положение аденина в последовательности GATC. В таком случае многие рестриктазы (например Bell, Mbol или Clal), в состав сайтов
рестрикции которых входит данная метилированная последовательность, перестают расщеплять ДНК по этим сайтам. Аналогичное действие на некоторые рестриктазы, например EcoRII, оказывает и dcm-метилаза, осуществляющая метилирование остатков цитозина по положению С5 в последовательностях CMeCAGG и CMeCTGG.
1.3.5.2 ДНК-лигазы
Создание фосфодиэфирных связей в одноцепочечных разрывах двухцепочечной ДНК с помощью ДНК-лигаз является, наряду с рестрикцией, одним из важнейших этапов получения рекомбинантных ДНК in vitro. Наибольшее применение в генно-инженерных исследованиях находит ДНК-лигаза бактериофага Т4. Реакция лигирования протекает в два этапа. Вначале образуется промежуточный комплекс фермент-АМР (этап 1), после чего остаток AMP переносится на 5'-фосфатную группу концевого нуклеотида в точке разрыва ДНК (этап 2). Образовавшаяся фосфодиэфирная связь гидролизуется во время нуклеофильной атаки З'-ОН группы соседнего нуклеотида, что приводит к образованию новой фосфодиэфирной связи, восстанавливающей целостность сахаро-фосфатного остова ДНК. Т4-ДНК- лигаза осуществляет соединение фрагментов двухцепочечной ДНК, обладающих комплементарными "липкими" или "тупыми" концами. Как следует из механизма реакции, необходимым условием протекания лигирования является наличие 5'-концевого фосфата и З'-концевого гидроксила в точках разрыва цепей ДНК. При этом эффективность соединения фрагментов ДНК по "тупым" концам Т4-ДНК-лигазой возрастает в присутствии Т4-РНК-лигазы, которая осуществляет ковалентное соединение 5'-фосфорилированных концов одноцепочечных ДНК или РНК с З'-ОН группами одноцепочечных нуклеиновых кислот.
1.3.6 Векторы
Ферменты, описанные в предыдущем разделе, позволяют производить тонкие манипуляции как с протяженными молекулами ДНК, так и с их фрагментами. В частности, с помощью рестриктаз можно с большой точностью разрезать молекулы ДНК, а образовавшиеся в результате фрагменты соединять в любой желаемой последовательности друг с другом, восстанавливая сахаро- фосфатный остов молекулы ДНК с помощью ДНК-лигазы. Однако с использованием только этих ферментов еще нельзя решить одну из основных методических задач молекулярной генетики - выделение любой требуемой нуклеотидной последовательности в чистом виде и в количестве, достаточном для исследования этих последовательностей биохимическими методами. Исключение составляет метод ПЦР, однако его применение ограничивается короткими последовательностями нуклеотидов.
Основная идея, позволяющая решать эту задачу, заключается в том, чтобы присоединить исследуемые фрагменты ДНК к молекуле-переносчику, которая могла бы автономно существовать внутри бактериальных или эукариотических клеток в виде одной или нескольких копий и передаваться вместе со встроенным в нее фрагментом ДНК от одной клетки к другой. Такие молекулы- переносчики фрагментов нуклеиновых кислот были созданы, их называют векторами, и они являются одним из важнейших инструментов генной инженерии.
Идеальная векторная молекула должна обладать несколькими обязательными свойствами. Во-первых, любой вектор должен длительное время существовать в популяции клеток-хозяев, т.е. реплицироваться автономно или вместе с хромосомами клеток. Во-вторых, в любом векторе должны быть биохимические или генетические маркеры, которые позволяли бы обнаруживать его присутствие в клетках. В-третьих, структура векторной молекулы должна допускать встраивание в нее чужеродной последовательности нуклеотидов без нарушения ее функциональной целостности. Для конструирования векторов в генной инженерии используют небольшие молекулы нуклеиновых кислот, способные к автономной репликации в бактериальных и эукариотических клетках - плазмиды, хромосомы вирусов, а также фрагменты хромосом эукариотических клеток /15, 16/.
Различные векторы для клонирования ДНК и их рестрикционные карты приведены на рисунке 1.4
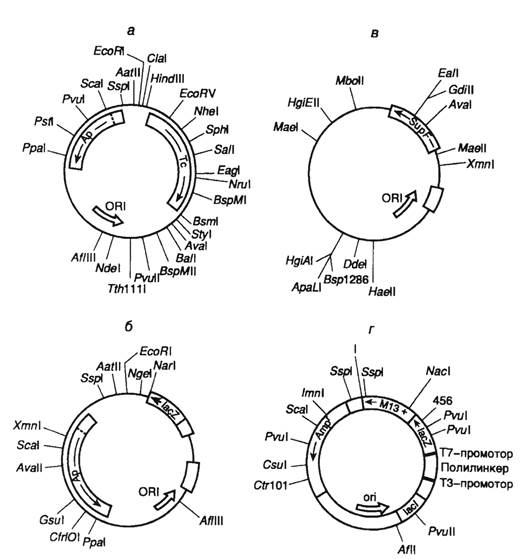
Первые эффективные векторы для клонирования фрагментов чужеродной ДНК, не утратившие своего значения и поныне, были получены с использованием бактериальных плазмид. Большая серия векторных плазмид, обозначенных символом pBR, создана на основе репликона природной плазмиды ColEI, придающей клеткам Е. coli устойчивость к колицину путем его объединения с генами устойчивости к антибиотикам. Таким образом, бактериальные клетки, несущие подобные комбинированные плазмиды, приобретали устойчивость к соответствующим антибиотикам, и их было легко отличить от бесплазмидных клеток путем простого посева на питательную среду с антибиотиками. Генетическая карта одного широко распространенного вектора этой серии - pBR322 изображена на рис. II.5,а.
Такая плазмида представляет собой кольцевую ковалентно замкнутую молекулу ДНК длиной 4363 и.о. Последовательность нуклеотидов pBR322 полностью известна. Плазмида содержит гены устойчивости к тетрациклину (Тс) и ампициллину (Ар), которые были перенесены в плазмиду pBR322 из плазмиды pSClOl и транспозона ТпЗ соответственно. Оба этих гена являются селектируемыми генетическими маркерами плазмиды, т.е. позволяют проводить отбор бактериальных клеток с плазмидой pBR322 по их способности к росту на питательных средах в присутствии тетрациклина и(или) ампициллина. Плазмида pBR322 содержит также обеспечивающий ее стабильную репликацию в клетках Е. coli участок ДНК, который включает область начала репликации (ori). Характерной чертой плазмиды pBR322, как и любого современного вектора, является наличие в ней нескольких уникальных сайтов рестрикции, обозначенных на генетической карте. Следует иметь в виду, что встраивание в плазмиду клонируемых чужеродных фрагментов ДНК по сайтам рестрикции, расположенным в генах Ар или Тс (например PstI или BamHI), будет нарушать целостность этих генов и их функциональную активность. В результате происходит утрата бактериальными клетками, содержащими рекомбинантные плазмиды, устойчивости к соответствующим антибиотикам.
