Страница
2
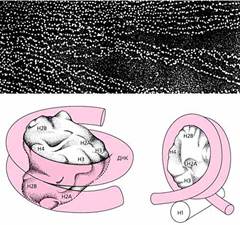
Электронная микрофотография хроматина (вверху) и модели минимальной (внизу слева) и полной нуклеосомы.
На фотографии хроматин виден как нить с нанизанными на нее бусинками. Ядро нуклеосомы, или минимальная нуклеосома, состоит из восьми молекул гистонов - по две молекулы каждого вида: Н2А, Н2В, Н3 и Н4. Этот октамер обвит сегментом ДНК, делающим вокруг ядра 1.75 оборота (внизу слева), а гистон-1 (Н1) в полной нуклеосоме “сшивает” ДНК в начале и в конце обвитого сегмента (внизу справа).
В нуклеосоме гистоны взаимодействуют с ДНК строго определенным образом. В начале 80-х годов в лаборатории А.Д.Мирзабекова был разработан метод анализа ДНК-белковых взаимодействий, основанный на сшивках этих молекул, с помощью которого удалось расшифровать порядок расположения гистонов в нуклеосоме [2]. Оказалось, что он одинаков в организмах, принадлежащих не только к разным видам, родам и классам, но даже царствам живой природы - грибам, растениям и животным. Это открытие объяснило высокую консервативность гистонов, необходимую для формирования столь сложного комплекса, какой представляет собой нуклеосома.

Хроматин в разной степени конденсации - на микрофотографии и на схеме.
В растянутой форме (нижняя часть рисунка) хроматин имеет вид нити с бусинками-нуклеосомами. За счет гистона-1 (Н1) он частично уплотняется, конденсируется (в середине), а затем конденсируется полностью (механизм остается неизвестным), и гены в этой части ДНК совершенно неактивны.
Большой вклад в формирование идей о нескольких уровнях упаковки ДНК в составе хроматина внесли работы Г.П.Георгиева и Ю.С.Ченцова [3]. Первый уровень - образование фибриллы диаметром 100 A; в ней ДНК становится компактнее в 6-7 раз. Далее при участии гистона-1 формируется 30-нанометровая фибрилла, в результате ДНК уплотняется еще в 20-50 раз. Существует огромное количество версий, объясняющих механизмы этих процессов, но до сих пор нет единого мнения на этот счет. Еще меньше известно об упаковке ДНК в петли и домены. Однако ни у кого нет сомнений в том, что структура нуклеосомы играет главную роль в укладке ДНК на всех уровнях. Именно взаимодействия между нуклеосомами определяют степень компактности ДНК.

Структура минимальной нуклеосомы (вид вдоль оси суперспирали ДНК). Разрешение 2.8 A
Показана половина нуклеосомы с одним витком суперспирали (73 пары оснований) и четырьмя молекулами гистонов (Н2А, Н2В, Н3, Н4). Их спиральные сегменты изображены в виде цилиндров, неструктурированные участки между ними - в виде петель, буквами N и С обозначены “хвосты”, т.е. аминные и карбоксильные концы молекул. Места, в которых ДНК контактирует с гистонами, указаны белыми крюками.
Рентгеноструктурный анализ, позволяющий получать данные о пространственном расположении атомов в кристалле, для нуклеосомы особенно сложен в силу того, что этот комплекс состоит из многих компонентов. Но в конце 90-х годов в лаборатории Т.Ричмонда такой анализ был успешно осуществлен и получено “изображение” структуры нуклеосомы с высоким разрешением - около 2.8 A [4]. Таким образом, появилась основа для более глубокого понимания тех механизмов, которые обеспечивают участие нуклеосомы в уплотнении ДНК и процессах регуляции генной активности на уровне хроматина.
Хвосты, хвосты, хвосты
Нуклеосома формируется по принципу многоуровневого узнавания, обусловленного строением гистонов. Молекула любого из них содержит центральный структурированный трехспиральный домен и неструктурированные N- и C-“хвосты”. Гистоны попарно узнают друг друга, и в этом важна роль особой гистоновой укладки. Спиральные домены взаимодействуют между собой, образуя структуры, названные рукопожатием, в результате чего возникают гетеродимеры - один Н3-Н4 и два Н2А-Н2В. Из первого димера в свою очередь образуется тетрамер (Н3)2-(Н4)2. Таким образом, этот тетрамер и два димера Н2А-Н2В составляют гистоновый октамер, сердцевину нуклеосомы.
Интересно, что мотив гистоновой укладки обнаружен во многих белках, которые активируют или подавляют считывание информации с ДНК. Из этого следует, что между структурой хроматина и механизмом транскрипции существует эволюционная связь.
Формой гистоновый октамер напоминает клин, благодаря чему обеспечивается левое закручивание спирали ДНК. На поверхности октамера, обращенной к ДНК, из центральных доменов формируются особые структурные элементы, или мотивы, которые можно разделить на три основных типа. Мотивы первого типа образованы -мостами - спаренными петлями гистоновых димеров. Мотивы второго типа - это спаренные N-концевые сегменты длинных спиральных доменов каждого гистона, образующего гетеродимер. Наконец, третий тип составляют два мотива из двух дополнительных a-спиральных участков гистона-3, расположенных вдоль суперспирали ДНК в месте ее входа в нуклеосому и выхода из нее. Поскольку перечисленные структурные элементы содержат положительно заряженные аминокислоты (в основном аргинины), октамер электростатически взаимодействует с отрицательно заряженными фосфатными группами сахарофосфатного остова ДНК. Таким образом, 14 малых бороздок ДНК втягивают в себя 14 содержащих аргинин мотивов гистонового октамера, расположенных на его поверхности. В результате ДНК жестко закрепляется почти независимо от нуклеотидной последовательности. Благодаря этому обеспечивается универсальность уплотнения ДНК на октамерах.
Итак, за счет консервативной центральной части гистонов формируется сам октамер и закрепляется ДНК, чем обеспечивается первый уровень ее уплотнения. ДНК оказывается на поверхности октамера и остается доступной для взаимодействия с другими белками.
Зачем же нужны гистоновые “хвосты”? Чтобы понять это, обратимся снова к нуклеосоме. Судя по рентгеноструктурному анализу, все они выходят на ее поверхность, причем “хвост” гистона-3 особенно далеко простирается за пределы нуклеосомы.
“Хвосты” гистонов очень подвижны. Выступая поверх не только нуклеосомы, но даже хроматиновой фибриллы, они участвуют в межнуклеосомном взаимодействии и подвергаются многочисленным модификациям. Среди них можно отметить ацетилирование, фосфорилирование, метилирование, AДФ-рибозилирование и присоединение белка убиквитина [5]. Эти модификации изменяют заряд, гидрофобность и другие свойства поверхности белковых глобул. Гистоновые “хвосты”, расположенные снаружи хроматиновой фибриллы, составляют до 25-30% от массы индивидуальных гистонов и различными заряженными группами мозаично “раскрашивают” поверхность монотонного хроматина. Кроме того, специализированные модифицирующие ферменты могут изменять эту мозаику, сочетая разные модифицирующие группы. Так формируется сложная матрица, которую узнают другие регуляторные белки, внешние сигналы. Более того, поскольку концевые домены гистонов участвуют и в межнуклеосомном взаимодействии, за счет модификаций хроматиновая фибрилла разрыхляется или, наоборот, уплотняется. Это, в свою очередь, облегчает или затрудняет доступ многочисленных регуляторов к ДНК.
