Страница
1
Процедура ионометрического титрования несложна. В анализируемую пробу, в которую погружены ионоселективный электрод и электрод сравнения, добавляется титрант, который связывает определяемое вещество. После каждой добавки записываются показания электродов. Кривая титрования в координатах E (потенциал электродов) от V (объем титранта) имеет ярко выраженный S-образный вид. Точка перегиба этой кривой является точкой эквивалентности (см. рис.1а). Если в анализируемом растворе присутствуют несколько определяемых ионов, то кривая имеет ступенчатый вид с несколькими точками перегиба. Каждая точка перегиба соответствует эквивалентному связыванию соответствующего определяемого иона (см. рис.1б).

Рис.1.
Помимо специфического вида кривых титрования, ионометрическое титрование носит характерные черты, о которых следует упомянуть.
Во-первых, процедура ионометрического титрования занимает гораздо больше времени, чем процедура классического титрования. Это связано с дополнительными кинетическими факторами, которые вносит пара электродов, так как на установление стабильного значения потенциала в окрестности точки эквивалентности уходит существенно больше времени, чем вне этой окрестности. Если не дожидаться установления стабильного значения потенциала, то погрешность анализа может быть большой.
Во-вторых, если стехиометрия вещества, образуемого в результате титрования, равна 1:1, кривая титрования должна быть центральносимметрична относительно точки эквивалентности. Это свойство является важным, так как большая часть аналитических методик разработана для соединений такого рода. Кривая титрования для соединений другой стехиометрии выглядит асимметрично.
В-третьих, ионометрическое титрование применяется для анализа в следующих случаях:
для определения с погрешностью меньшей 0,5%;
для определения нескольких ионов одновременно;
для проведения анализа в присутствии таких количеств мешающих ионов, при которых определение методам градуировочного графика и стандартных добавок невозможно.
Важное место в процедуре титрования составляют математические методы нахождения точки эквивалентности. Наибольшее распространение получили 2 способа определения положения точки эквивалентности.
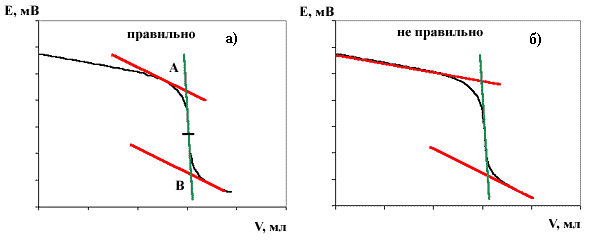
Первый способ состоит в нахождении центра симметрии кривой титрования, исходя из того, что в окрестности точки эквивалентности кривая центральносимметрична. Для нахождения центра симметрии проводится 3 прямые. Две прямые параллельны друг другу и являются касательными к некоторым участкам кривой титрования (см. на рис.2а красные линии). Чем ближе эти прямые будут находиться к точке эквивалентности, тем лучше. Третья прямая аппроксимирует точки около точки эквивалентности (см. зеленую линию). Если получившийся отрезок АB разделить пополам, то найденная точка является искомой точкой эквивалентности. Некоторые экспериментаторы предпочитают обрабатывать кривые титрования так, как это показано на рисунке 2б. Когда кривая титрования не идеально симметрична, то такая обработка результатов ошибочна, так как теряется математический смысл операции, а значит погрешность определения может быть ощутимой.
|
|
|
Рис.2. |
Второй способ состоит в численном дифференцировании кривой титрования. Максимум (минимум) дифференциальной кривой находится в точке эквивалентности (см. рис.3). Самый простой способ дифференцирования состоит в вычислении отношения разностей между 2-мя соседними экспериментальными точками кривой титрования. Иными словами, для каждой соседней пары точек вычисляется следующее отношение: (Еi+1 - Ei)/(Vi+1 - Vi), где Ei - потенциал ионоселективного электрода после добавки титранта объемом Vi. Каждому вычисленному значению, а это будет ордината будущего графика, соответствует значение абсциссы, которая определяется как среднее арифметическое (Vi+1 + Vi)/2.
|
|
|
Рис.3. |
Безусловно, для нахождения точки эквивалентности асимметричных кривых титрования дифференциальный метод предпочтительней. Однако дифференциальный метод имеет и негативные стороны. Во-первых, усложняется процедура расчетов. Во-вторых, требуется большая частота экспериментальных точек в окрестности точки эквивалентности, что не всегда бывает удобно.
Описанные выше способы расчетов предполагают, что титрование в окрестности точки эквивалентности должно проводиться малыми порциями титранта, чтобы не пропустить максимальный скачок потенциала. Такое положение дел выглядит парадоксально, поскольку обилие экспериментальных точек должно вносить какие-нибудь преимущества в процедуру анализа. На деле же не наблюдается почти никаких ощутимых преимуществ в сравнении с классическим титрованием. Выходом из положения могло бы быть знание функциональной закономерности, описывающей кривую титрования. Однако часто бывает так, что нельзя точно знать заранее вид кривой титрования.
Мною разработан новый способ расчета, который позволяет несколько уменьшить важность экспериментальных точек в окрестности точки эквивалентности. Расчеты проводятся 2 этапа. Первый этап состоит в вычислении нескольких значений точки эквивалентности, используя несложную процедуру. Второй этап состоит в экстраполяции полученных значений, с целью получения истинного значения точки эквивалентности.
Процедура вычисления единичного значения эквивалентного объема похожа на процедуру численного дифференцирования, которая была описана выше. Различие состоит только в том, что производится вычисление не отношения разностей, а разность потенциалов кривой титрования. Разность вычисляется не между соседними экспериментальными точками, а между точками, отстоящими друг от друга на расстояние V, заданное ранее. Также как и дифференциальная, полученная кривая имеет экстремум, абсцисса которого является точкой эквивалентности. Производя вычисления при различных значениях V, получаем несколько значений точки эквивалентности, экстраполируя которые можно получить истинное значение. Экстраполяция производится на графике в координатах Vэкв от V, где Vэкв - значение эквивалентного объема, полученное при заданном V. Так как вид графика может быть непредсказуемо разнообразным, то экстраполировать на ось ординат следует только начальные точки графика (см. на рис.4 красную линию).
|
|
|
Рис.4. |
Помимо необходимой информации об эквивалентном объеме, график содержит не менее важные сведения о благополучии проведенного анализа. Это так, поскольку график отражает меру асимметрии кривой титрования. В свою очередь симметрия, или асимметрия в определенных границах, свидетельствует о правильности выполненного анализа. Характеристикой асимметрии может служить наклон экстраполирующей прямой.