Определение массовой доли вещества

Oтвет: M(CrCl3) = 25,0%.
Задача 7. При гидролизе средней соли образовалось 20,4г вещества H2X, массовая доля водорода в котором равна 5,88%, и 41,2 г вещества M(OH)3, массовая доля M в котором равна 50,49%. Oпределите формулу соли.
Pешение
1. Для определения элемента X находим массу и количество вещества элементов водорода и X, содержащихся в 20,4 г вещества H2X, а также молярную массу элемента X:
![]()
m(X) = 20,4 г - 1,2 г = 19,2 г;
![]()
![]()
следовательно, X — это сера.
2. Определяем массу элемента М:
![]()
то(М)ж41,2г 0,5049ж20,8 г.
3. Так как количество вещества элемента М и количество вещества M(OH)3 равны, то составим уравнение и определим элемент М, обозначив его молярную массу через
![]()
Решая уравнение, находим, что - = 52 г/моль, следовательно, элемент М — это хром.
4. Для определения формулы соли необходимо знать количество вещества элементов серы и хрома:
![]()
следовательно, формула соли Cr2S3. Ответ: Cr2S3.
Задача 7. Газ, образовавшийся при разложении дихромата аммония массой 126 г, смешали с газом, выделившимся при растворении 42 г гидрида натрия в 900 мл 2 M раствора хлороводорода, и пропустили при соответствующих условиях над никелевым катализатором. Продукт реакции растворили в избытке раствора азотной кислоты. Рассчитайте, насколько увеличится масса раствора азотной кислоты.
Решение
1. Масса азотной кислоты увеличивается за счет поглощения аммиака, который образуется при соответствующих условиях из водорода и азота:
(1) (2)
(3)  (4)
(4)
2. Найдем количество вещества азота:
![]()
3. Определим количество вещества водорода:
![]()
ra(HCl) ж 2 моль/л 0,9 л ж 1,8 моль — избыток, значит, количество вещества водорода определяем по NaH:
ra(H2)ζ ra(NaH) ж 1,75 моль.
4. Сравним количество вещества N2 и H2. По уравнению:
![]()
а имеем 0,5 моль, следовательно, азот прореагирует полностью.
5. Вычислим массу аммиака:
ra(NH3)ζ 2ra(N2)ζ 1моль; то(NH3)ζ 1 моль ■ 17 г/моль ж 17 г — на столько увеличится масса раствора азотной кислоты. Ответ:![]() ж 17 г.
ж 17 г.
Задача 8. К раствору хлорида железа, содержащему 13,0 г соли, прибавили избыток гидроксида калия. При этом образовался осадок массой 8,56 г. Определите валентность железа в хлориде.
Решение
1. Известны нераствормые гидроксиды железа(11) и железа(Ш). Обозначим валентность железа в хлориде через,:
![]()
2. Выразим через & количество вещества соли и гидроксида железа:
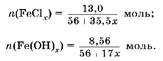
3. вставим уравнение:

Pешая уравнение, получаем, что валентность железа в хлориде равна III.
Oтвет: III.
Задача 9. Cмесь металла и сульфида данного металла полностью растворилась в 10%-ной соляной кислоте, при этом выделилось 11,2 л (н. у.) газа. При добавлении к образовавшемуся раствору раствора красной кровяной соли образуется осадок синего цвета. При пропускании выделившегося газа через избыток раствора нитрата свинца образуется 47,8 г осадка черного цвета. Oпределите массовые доли компонентов смеси.
Pешение
1. Исходная смесь полностью растворилась в соляной кислоте, следовательно, и металл, и сульфид данного металла прореагировали нацело. Взаимодействие с красной кровяной солью с образованием осадка синего цвета (турнбулевой сини) — качественная реакция на катион Fe2K, следовательно, металл — железо, сульфид металла — FeS:

2. Hайдем массу сульфида железа: 
3. Oпределим массу железа:
Ai(H2) = га(газов) - Ai(H2S); Ai(H2) = 0,5 моль - 0,2 моль = 0,3 моль; Ai(Fe) = (H2) = 0,3моль; An(Fe) = 0,3 моль ■ 56 г/моль = 16,8 г.
4. Вычислим массовые доли компонентов смеси:
т(см.) = 16,8 г K 17,6 г = 34,4 г;
![]()
M(Fe) = 100%- 51,16%=48,84%. Oт в е т: M(Fe) = 48,84%; M(FeS) = 51,16%.
Задача 6.334. Cмесь железа и магния обработали концентрированной серной кислотой и собрали газ объемом 1,68 л (н. у.). ^ра-створившийся остаток отделили и обработали разбавленной азотной кислотой, при этом остаток полностью растворился. Полученный раствор осторожно выпарили, соль прокалили. Масса твердого остатка составила 12 г. Oπределите количественное соотношение металлов в смеси.
Pешение
1. Железо при обычных условиях с концентрированной серной кислотой не взаимодействует, но растворяется в разбавленной азотной кислоте с образованием нитрата железа(Ш):

2. Вычислим количество вещества магния:
![]()
3. Вычислим количество вещества железа: 
4. Определим соотношение металлов в смеси:!(Fe): Ti(Mg) ж 0,15: 0,3 ж 1: 2. Ответ: ra(Fe): ra(Mg) ж 1: 2.
Задача 10. Навеску смеси порошкообразных хрома и марганца обработали хлором без нагревания, масса навески при этом увеличилась на 2,13 г. Полученную смесь растворили в воде. Нерастворившийся твердый остаток отделили и обработали при нагревании концентрированной серной кислотой. Выделившийся газ был поглощен 60 мл 0,2 M раствора перманганата калия. Вычислите массу исходной навески.
Решение
1. С хлором без нагревания взаимодействует только марганец, при этом образуется соль MnCl2, растворимая в воде. С концентрированной серной кислотой при нагревании взаимодействует хром, причем образуется сульфат хрома(Ш) и выделяется SO2, который и взаимодействует с перманганатом калия:

2. Найдем массу марганца:
![]()
то(Мп) ж 0,03 моль ■ 55 г/моль ж 1,65 г.
3. Найдем массу хрома:

TO(Cr) ж 0,02 моль ■ 52 г/моль ж 1,04 г.
