Медь и её сплавы
Соединения элементов подгруппы меди распределены в земной коре неравномерно, что объясняется различием в геологических условиях, сложившихся в различных местах земного шара. Богатейшие месторождения меди имеются в Конго (Катангский пояс). Материалы, собранные археологами о древнейших месторождениях датируются тысячелетиями до новой эры. Древнейшие выработки меди на территории нашей страны найдены в Закавказье, на побережье Балхаша, в многочисленных пунктах Сибири.
Планомерные поиски месторождений меди начинаются при Иване III, Иване Грозном и особенно при Петре I. При Иване Грозном в Олонецкий уезд был послан новгородский гость (купец) Семен Гаврилов “для сыску медные руды”, где она и была найдена. В 1652 г. Казанский воевода сообщил царю: “Медные руды… сыскано много и заводы к медному делу заводим”. [2, с.26] Из документов следует, что с 1562 по 1664 г. было послано из “Казани к Москве чистыя меди 4641 пуд. 6 гривенков”. В 1702 г. стала выходить первая русская газета “Ведомости”, которую, очевидно, редактировал Петр I. 2 января 1703 г. в ней писали: “Из Казани пишут. На реке Соку нашли много нефти и медной руды, из той руды меди выплавили изрядно, отчего чают не малую прибыль Московскому государству”.
В начале этого столетия главнейшими месторождениями, которые разрабатывались, были: в районе Северного Урала – Богословский завод, в районе Нижнего Тагила – Выйский завод, а на Кавказе – Калакентский и Кедабекский заводы.
В наше время известны месторождения меди на восточном склоне Урала, Средней Азии, Закавказье и т.д.
Большое количество меди и других ископаемых находится на дне океанов, которое покрыто так называемыми конкрециями – скоплениями в виде камней округлой неправильной формы. Они содержат в среднем 0,5% меди. По подсчетам ученых запасы этой ценной и своеобразной руды составляют 5 млрд. тонн.
Физические и химические свойства меди
Физические свойства
Металлы подгруппы меди, как и щелочные металлы, имеют по одному свободному электрону на один ион-атом металла. Казалось бы, эти металлы не должны особенно сильно отличатся от щелочных. Но они, в отличие от щелочных металлов, обладают довольно высокими температурами плавления. Большое различие в температурах плавления между металлами этих подгрупп объясняется тем, что между ион-атомами металлов подгруппы меди почти нет “зазоров” и они расположены более близко. Вследствие этого количество свободных электронов в единице объема, электронная плотность, у них больше. Следовательно, и прочность химической связи у них больше. Поэтому металлы подгруппы меди плавятся и кипят при более высоких температурах.
Металлы подгруппы меди обладают, по сравнению с щелочными металлами, обладают большей твердостью. Объясняется это увеличением электронной плотностью и отсутствием “зазоров” между ион-атомами.
Необходимо отметить, что твердость и прочность металлов зависят от правильности расположения ион-атомов в кристаллической решетке. В металлах, с которыми мы практически сталкиваемся, имеются различного рода нарушения правильного расположения ион-атомов, например пустоты в узлах кристаллической решетки. К тому же металл состоит из мелких кристалликов (кристаллитов), между которыми связь ослаблена. В Академии Наук СССР была получена медь без нарушения в кристаллической решетке. Для этого очень чистую медь возгоняли при высокой температуре в глубоком вакууме на глубокую подложку. Медь получалась в виде небольших ниточек – “усов”. Как оказалось такая медь в сто раз прочнее, чем обычная.
Цвет меди и её соединений
Чистая медь обладает и другой интересной особенностью. Красный цвет обусловлен следами растворенного в ней кислорода. Оказалось, что медь, многократно возогнанная в вакууме (при отсутствии кислорода), имеет желтоватый цвет. Медь в полированном состоянии обладает сильным блеском.
При повышении валентности понижается окраска меди, например CuCl – белый, Cu2O – красный, CuCl + H2O – голубой, CuO – черный. Карбонаты характеризуются синим и зеленым цветом при условии содержания воды, чем обусловлен интересный практический признак для поисков.
Электропроводимость
Медь обладает наибольшей (после серебра) электропроводимостью, чем и обусловлено её применение в электронике.
Медь кристаллизируется по типу централизованного куба (рис 1).
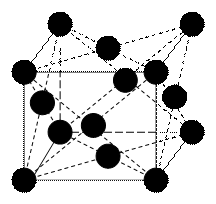
Рисунок 1. Кристаллическая решетка меди.
Характеристики основных физико-механических свойств меди
| Плотность r , кг/м3 | 8890 |
| Температура плавления Тпл, ° С | 1083 |
| Скрытая теплота плавления D Нпл, Дж/г | 208 |
| Теплопроводность l , Вт/ (м × град), при 20–100 ° С | 390 |
| Удельная теплоемкость Ср, Дж/ (г × К), при 20–100 ° С | 0,375 |
| Коэффициент линейного расширения a × 10–6, град–1, при 0–100 ° С | 16,8 |
| Удельное электросопротивление r × 108, Ом × м, при 20–100 ° С | 1,724 |
| Температурный коэффициент электросопротивления, град–1, при 20–100 ° С | 4,3× 10–3 |
| Предел прочности s в, МПа | |
| мягкой меди (в отожженном состоянии) | 190-215 |
| твердой меди (в нагартованном состоянии) | 280-360 |
| Относительное удлинение d , % | |
| мягкой меди (в отожженном состоянии) | 60 |
| твердой меди (в нагартованном состоянии) | 6 |
| Твердость по Бринеллю НВ, МПа | |
| мягкой меди (в отожженном состоянии) | 45 |
| твердой меди (в нагартованном состоянии) | 110 |
| Предел текучести s t , МПа | |
| мягкой меди (в отожженном состоянии) | 60-75 |
| твердой меди (в нагартованном состоянии) | 280-340 |
| Ударная вязкость KCU, Дж/см2 | 630-470 |
| Модуль сдвига G × 10–3, МПа | 42-46 |
| Модуль упругости Е × 10–3, МПа | |
| мягкой меди (в отожженном состоянии) | 117-126 |
| твердой меди (в нагартованном состоянии) | 122-135 |
| Температура рекристаллизации, ° С | 180-300 |
| Температура горячей деформации, ° С | 1050-750 |
| Температура литья, ° С | 1150-1250 |
| Линейная усадка, % | 2,1 |
