Исследование систем возбуждения эксимерных лазеров на основе LC-контура
Табл.1. Положения резонансов (Эв) для термов автораспадных состояний
|
Терм |
F2 |
Cl2 |
Br2 |
I2 |
|
2Σ+u |
0.09 |
- |
- |
- |
|
2Пg |
4 |
0.03 |
0.07 |
0.05 |
|
2Пu |
7 |
2.5 |
1.4 |
0.9 |
|
2Σ+g |
10 |
5.5 |
3.7 |
2.5 |
Как видно, за исключением молекулы фтора, основной терм молекулярного иона не пересекается с термом основного состояния молекулы согласно [29].Из данных представленных в табл.3 следует, что сечение захвата электрона молекулами Сl2, Вг2 и I2 должно быть меньше, чем в случае молекулы F2. Это противоречит некоторым экспериментам, так что поведение термов в соответствии с данными табл. 8 требует дополнительной проверки.
В табл.2 содержатся энергетические параметры и константа скорости процессов (18) и (19) при тепловых столкновениях
Табл.2. Константа скорости прилипания электрона kat к
молекулам галогенов в области температур 300 – 350
|
Молекула |
Энергия сродства молекулы к электрону (Эв) |
Энергия сродства атома галогенида к электрону (Эв) |
kat, 10-10 см3/с |
|
HCl(ν=0) |
- |
3.62 |
1-6 |
|
HCl(ν=1) |
- |
3.62 |
30-60 |
|
HCl(ν=2) |
- |
3.62 |
300-800 |
|
F2 |
3 |
3.4 |
30-70 |
|
Сl2 |
2.4 |
3.62 |
2-37 |
|
Вг2 |
2.5 |
3.36 |
0.008-1.3 |
|
I2 |
2.5 |
3.06 |
1.4-92 |
Отметим большой разброс данных. Сечение прилипания электрона к молекуле хлора как функция энергии электрона представлено на рис.14,а. Наблюдаемый резонанс при малых энергиях электрона свидетельствует о пересечении терма автораспадного состояния Сl-2 (2Σ+u) и молекулярного терма, что противоречит данным табл.1. Зависимость от энергии для константы скорости прилипания электрона к молекуле фтора приведена на рис.14,б).
В заключении отметим, что концепция прилипания электронов к молекулам через образование автораспадных состояний существует несколько десятилетий и является основой для понимания этих процессов. Экспериментальные исследования привели к более глубокому представлению об этих процессах и позволили проанализировать процессы прилипания электрона не только к газовым молекулам, но и к другим атомным системам, включающим комплексы, кластеры и пленки. Поэтому современные знания о процессах прилипания электрона могут быть полезны для анализа различных явлений на границе плазмы и поверхности, а также на поверхности частицы, находящейся в плазме.
Прилипание электронов к двухатомным молекулам
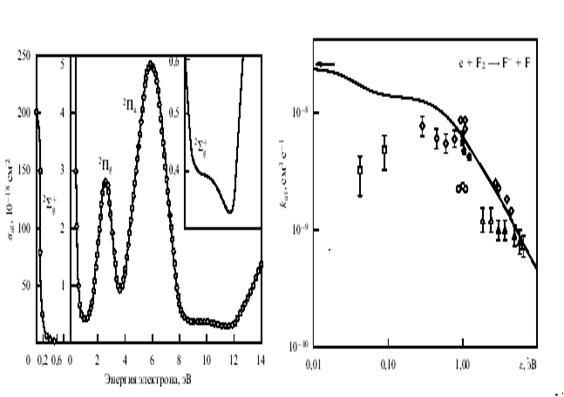
а) б)
Сечение диссоциативного прилипания электрона
к молекуле хлора – а).
Константа скорости диссоциативного прилипания электрона
к молекуле фтора по данным разных работ – б).
Рис.14
3. Динамика предыонизации.
Прилипание электрона к молекулам, носит чрезвычайно сложный характер и протекает, как упоминалось выше через образование автораспадных состояний полной системы. В связи с резонансной природой такие процессы характеризуются большими сечениями или константами скоростей и поэтому представляют интерес для различных плазменных систем. Процесс прилипания электрона используется в эксимерных лазерах и эксилампах для быстрого получения атомов фтора и хлора из различных галогенсодержащих молекул. Сечение прилипания электронов к молекуле HCl зависит от ее колебательного состояния (см. Табл.2).
Процесс возбуждения молекулы HCl в активной среде в (к основным электродам не приложено напряжение и действует только стационарный источник предыонизации) описывается следующей системой кинетических уравнений:
 (21)
(21)
где k0a, k1a, k2a – скоростные коэффициенты диссоциативного прилипания прилипания электрона к молекуле в разных колебательных состояниях, соответственно ν=0, ν=1, ν=2. Cкоростные коэффициенты возбуждения электронами колебательных уровней молекулы и основного состояния обозначены как k01, k02. Производительность источника прдыонизации считается постоянной и равной I. Ne, No, N1, N2 концетрации электронов и HCl. Скорость рекомбинации – γ. Допускалось, что средняя энергия электронов постоянна и скоростные коэффициенты брались из работы [29-31]. Для упрощения во внимание принимались только наиболее интенсивные каналы возбуждения колебательных состояний молекулы HCl. Эффективная частота прилипания η при этом зависит от времени и равна:
η(t)=![]() (22)
(22)
Система уравнений (21) решалась численно с помощью стандартных программ MathCad. При этом использовались величина концентрации HCl типичная для эксимерных лазеров. На рис.15-17 представлены зависимости от времени концентраций электронов и молекул HCl в разных колебательных состояниях. Температура газа считалась равной Т=300 К и поэтому начальные концентрации молекулы HCl в возбужденных колебательных состояниях брались равными:
